题目内容
Ⅰ浓度为0.1mol?L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+)依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小的顺序是
(2)完全中和一定量NaOH溶液时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为
(3)与锌反应开始时产生氢气的速率分别为v1、v2、v3,其由大到小的顺序是
Ⅱc(H+)相同的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液均加水稀释至体积为原来的10倍,c(H+)依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小的顺序是
(2)三种溶液体积相同时,同时加入相同的锌,若产生相同物质的量的氢气,所需时间分别为t1、t2、t3,其大小关系是
(1)三种溶液中c(H+)依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小的顺序是
bac
bac
.(2)完全中和一定量NaOH溶液时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为
V1=2V2=V3
V1=2V2=V3
.(3)与锌反应开始时产生氢气的速率分别为v1、v2、v3,其由大到小的顺序是
v2>v1>v3
v2>v1>v3
.Ⅱc(H+)相同的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液均加水稀释至体积为原来的10倍,c(H+)依次为a mol?L-1,b mol?L-1,c mol?L-1,其由大到小的顺序是
c>b=a
c>b=a
.(2)三种溶液体积相同时,同时加入相同的锌,若产生相同物质的量的氢气,所需时间分别为t1、t2、t3,其大小关系是
t1=t2>t3
t1=t2>t3
.分析:I(1)盐酸和硫酸是强酸,醋酸是弱酸;
(2)根据酸与碱反应方程式中的关系分析;
(3)根据溶液中氢离子浓度分析;
II.
(1)醋酸是弱电解质,存在电离平衡,加水促进电离;
(2)由于醋酸存在电离平衡,与Zn反应时氢离子浓度减小的慢,所以反应速率快;
(2)根据酸与碱反应方程式中的关系分析;
(3)根据溶液中氢离子浓度分析;
II.
(1)醋酸是弱电解质,存在电离平衡,加水促进电离;
(2)由于醋酸存在电离平衡,与Zn反应时氢离子浓度减小的慢,所以反应速率快;
解答:解:I(1)盐酸是一元强酸完全电离,其氢离子浓度为:0.1mol?L-1,硫酸是二元强酸完全电离,其氢离子浓度为:0.2mol?L-1,醋酸是弱酸部分电离,其氢离子浓度小于0.1mol?L-1,所以氢离子浓度由大到小的顺序是bac,故答案为:bac;
(2)HCl+NaOH=NaCl+H2O,H2SO4+2NaOH=Na2SO4+2H2O,CH3COOH+NaOH=CH3COONa+H2O根据盐酸、硫酸、醋酸与NaOH溶液反应的方程式可知,硫酸与氢氧化钠反应时消耗的硫酸体积最小,盐酸和醋酸与氢氧化钠反应时消耗体积相同,所以V1=2V2=V3;故答案为:V1=2V2=V3;
(3)氢离子浓度越大反应速率越快,已知氢离子浓度由大到小的顺序是bac,所以与锌反应开始时产生氢气的速率由大到小的顺序:v2>v1>v3;故答案为:v2>v1>v3;
II.(1)醋酸是弱电解质,存在电离平衡,加水促进电离,氢离子的物质的量增大,均加水冲稀10倍后,醋酸中氢离子浓度大于盐酸和硫酸,所以氢离子浓度由大到小的顺序是c>b=a;故答案为:c>b=a;
(2)由于醋酸存在电离平衡,与Zn反应时氢离子浓度减小的慢,所以反应速率快,所用时间最短,盐酸和硫酸中氢离子相同反应速率相同,所需时间大小关系:t1=t2>t3;故答案为:t1=t2>t3.
(2)HCl+NaOH=NaCl+H2O,H2SO4+2NaOH=Na2SO4+2H2O,CH3COOH+NaOH=CH3COONa+H2O根据盐酸、硫酸、醋酸与NaOH溶液反应的方程式可知,硫酸与氢氧化钠反应时消耗的硫酸体积最小,盐酸和醋酸与氢氧化钠反应时消耗体积相同,所以V1=2V2=V3;故答案为:V1=2V2=V3;
(3)氢离子浓度越大反应速率越快,已知氢离子浓度由大到小的顺序是bac,所以与锌反应开始时产生氢气的速率由大到小的顺序:v2>v1>v3;故答案为:v2>v1>v3;
II.(1)醋酸是弱电解质,存在电离平衡,加水促进电离,氢离子的物质的量增大,均加水冲稀10倍后,醋酸中氢离子浓度大于盐酸和硫酸,所以氢离子浓度由大到小的顺序是c>b=a;故答案为:c>b=a;
(2)由于醋酸存在电离平衡,与Zn反应时氢离子浓度减小的慢,所以反应速率快,所用时间最短,盐酸和硫酸中氢离子相同反应速率相同,所需时间大小关系:t1=t2>t3;故答案为:t1=t2>t3.
点评:本题考查的重点是弱电解质的电离知识,注意弱电解质的电离平衡的移动情况,难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
从2L 1mol?L-1的NaOH溶液中取100ml,有关这100ml溶液的叙述中错误的是( )
| A、浓度为0.1mol?L-1 | B、浓度为1mol?L-1 | C、含4g NaOH | D、含0.1mol NaOH |

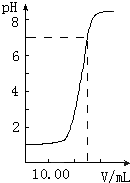 如图是向20.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH值变化的图象,根据图象分析,下列结论中不正确的是( )
如图是向20.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH值变化的图象,根据图象分析,下列结论中不正确的是( )