题目内容
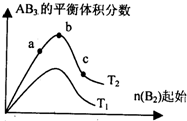 在其他条件不变时,改变某一条件对反应:A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图变化规律(图中T表示温度,n表示物质的量),根据图示可得出的结论正确的是( )
在其他条件不变时,改变某一条件对反应:A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图变化规律(图中T表示温度,n表示物质的量),根据图示可得出的结论正确的是( )| A、正反应一定是放热反应 | B、达到平衡时A2的转化率大小为:b>a>c | C、若T2>T1,则正反应一定是吸热反应 | D、b点时,平衡体系中A、B原子数之比可能接近1:3 |
分析:由图可知,B2起始相同时,平衡时温度T2对应的AB3的含量大,则若该正反应为吸热反应,则T2>T1,若该正反应为放热反应,则T2<T1;B2越大,达到平衡时A2的转化率越大,且b点AB3的体积分数最大,则反应物的物质的量之比接近等于化学计量数之比,以此来解答.
解答:解:A.该反应无法确定是吸热反应还是放热反应,故A错误;
B.由图可知,横坐标为B2的物质的量,增大一种反应物的量必然会促进另一种反应物的转化,则B2越大达到平衡时A2的转化率越大,即达到平衡时A2的转化率大小为c>b>a,故B错误;
C.由图可知,B2起始相同时,T2对应的AB3的含量大,若T2>T1,则该正反应为吸热反应,故C正确;
D.b点AB3的体积分数最大,则反应物的物质的量之比接近等于化学计量数之比,反应物均为双原子分子,所以平衡体系中A、B原子数之比接近1:3,故D正确;
故选CD.
B.由图可知,横坐标为B2的物质的量,增大一种反应物的量必然会促进另一种反应物的转化,则B2越大达到平衡时A2的转化率越大,即达到平衡时A2的转化率大小为c>b>a,故B错误;
C.由图可知,B2起始相同时,T2对应的AB3的含量大,若T2>T1,则该正反应为吸热反应,故C正确;
D.b点AB3的体积分数最大,则反应物的物质的量之比接近等于化学计量数之比,反应物均为双原子分子,所以平衡体系中A、B原子数之比接近1:3,故D正确;
故选CD.
点评:本题考查化学反应速率及化学平衡图象,明确横坐标为反应物B2的物质的量及该反应可能为吸热反应,也可能为放热反应是解答本题的关键,题目难度较大,为易错题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
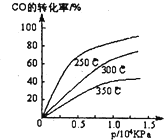 工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)
工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g) CH3OH(g) ΔH< 0
CH3OH(g) ΔH< 0
 CH30H(g)
CH30H(g)