题目内容
一定体积的溶质质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质的质量分数恰好增大1倍,溶液体积变为62.5 mL。则浓缩后溶液的物质的量浓度为( )。
A.2.2 mol·L-1 B.4 mol·L-1 C.5 mol·L-1 D.6.25 mol·L-1
B
【解析】设原溶液的质量为x g,所含氢氧化钾的质量为y g。根据溶质的质量分数概念可以列①式: =14%,其蒸发掉50 g水后,溶液的质量为(x-50)g;根据溶质的质量分数概念可以列②式:
=14%,其蒸发掉50 g水后,溶液的质量为(x-50)g;根据溶质的质量分数概念可以列②式: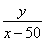 =28%。联立①②两式解得x=100,y=14,故n(KOH)=0.25 mol。c(KOH)=
=28%。联立①②两式解得x=100,y=14,故n(KOH)=0.25 mol。c(KOH)=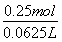 =4 mol·L-1。
=4 mol·L-1。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下表为四种溶液的溶质质量分数和物质的量浓度的数值,根据表中数据判断四种溶液中密度最小的是( )。
溶液 | KOH | HNO3 | CH3COOH | HCl |
溶质质量分数w(%) | 56 | 63 | 60 | 36.5 |
物质的量浓度c(mol·L-1) | 14.3 | 13.8 | 10.6 | 11.8 |
A.HCl B.HNO3 C.CH3COOH D.KOH