题目内容
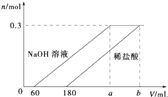
【题目】一块表面被氧化的铝分成两等分,若向其中一份中滴加1molL-1的NaOH溶液,向另一份中滴加x molL-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )
A. a=260
B. x=1mol/L
C. 该铝块的总质量为8.46g
D. 该铝块中氧化铝与铝单质的物质的量之比为3:20
【答案】C
【解析】分析可知,铝与盐酸、铝与氢氧化钠都是2 mol铝产生3 mol氢气;A、产生0.3mol氢气,消耗0.2mol氢氧化钠,NaOH的浓度是1mol/L,V(NaOH)=200mL,加上与氧化铝反应的60mL,求出a=260,A项正确;B、预想求出稀盐酸的浓度x,需利用2mol NaOH~1molAl2O3的关系求出n(Al2O3)=0.03mol,再根据1molAl2O3~6HCl,求出n(HCl)=0.18mol,x=1mol/L,B项正确;C、与NaOH反应的Al2O3是0.03mol,产生0.3mol氢气,需要0.2mol铝,一份铝块的质量=m(Al2O3)+m(Al)=8.46g,总质量为8.46![]() 2=16.92g,C项错误; D、根据与氢氧化钠反应的氧化铝0.03mol,与氢氧化钠反应的铝0.2mol,所以氧化铝与铝单质的物质的量之比为3:20,D项正确;答案选C。
2=16.92g,C项错误; D、根据与氢氧化钠反应的氧化铝0.03mol,与氢氧化钠反应的铝0.2mol,所以氧化铝与铝单质的物质的量之比为3:20,D项正确;答案选C。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目