题目内容
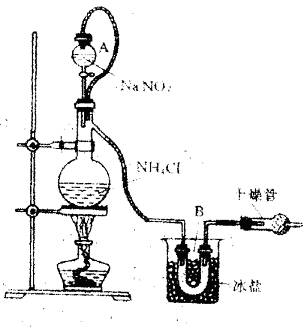
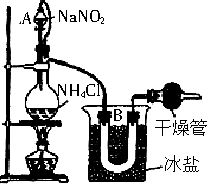
(1)实验室常用饱和NaNO2和NH4Cl溶液反应制取纯净氮气,反应式为:NaNO2+NH4Cl=NaCl+N2↑+2H2O↑△H=-Q
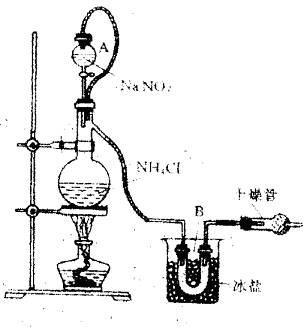
实验装置如图所示,试回答:
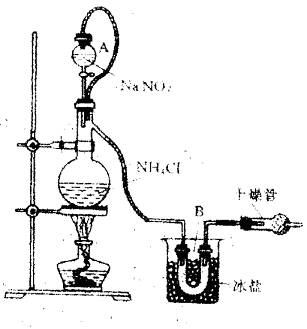
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是 (填写编号)
a.防止NaNO2饱和溶液蒸发
b.保证实验装置不漏气
c.使NaNO2饱和溶液容易滴下
②B部分的作用是 。
a.冷凝 b.冷却氮气 c.缓冲氮气流
③加热前必须进行的一个操作步骤是 ,加热片刻后,即应移去酒精灯以防反应物冲出,其原因是 。
④收集N2前,必须进行的步骤是(用文字说明) ,收集N2最适宜的方法是(填写编号)
a.用排气法收集在集气瓶中
b.用排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中
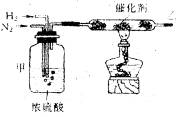
(2)实验室合成氨装置如图所示,试回答:装置甲的作用是:① , ② 。

(3)从乙处导出的气体是 ,检验产物的简单化学方法是 。
答案:
解析:
提示:
解析:
| (1)① c ② a ③检查装置的气密性;本反应为放热反应 ④将系统内的空气排尽;c
(2)①干燥气体 ②使两种气体充分混合 ③观察气泡以调节氢气、氮气气流速率 (3)氨及氮气、氢气的混合物;用蘸有浓盐酸的玻璃棒放在导管口,有白烟说明有氨生成
|
提示:
| (1)从反应式看,发生反应时,烧瓶中的压力必然比分液漏斗A中大,因而使A中NaNO2溶液不易滴入烧瓶中。如果将A与烧瓶间用导管连接,可以使A与烧瓶中压力始终保持相同,有利于NaNO2溶液滴入烧瓶中。由于是液体与液体反应制气,又是放热反应,因此气体产物N2中一定含有大量水蒸气。通过冰盐致冷剂后,可将大部分水蒸气冷凝。制气反应在反应前必须检查装置的气密性。该反应是放热反应,反应一旦启动,就不必再继续加热,否则会由于反应过于激烈而使反应物冲出。由于实验目的是制纯净氮气,因而在收集N2前必须将系统内的空气排尽。从提供的三种收集N2方法看,最适宜的方法是直接收集在球胆或塑料袋中。
(2)从装置看,瓶甲中装有浓H2SO4,起到干燥气体的作用。从图中气泡提示,通过观察气泡产生的情况来控制气流的速度。反应气体可以在瓶甲的空间部分充分混合。 (3)题目中已给出的是合成氨装置,瓶乙处导出的气体必然含NH3。检验氨最简便的方法是用蘸有浓盐酸的玻璃棒接近导管口,有白烟(微小的NH4Cl晶体)发生,说明有氨生成。
|

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目