题目内容
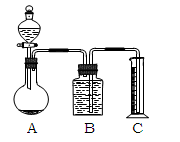
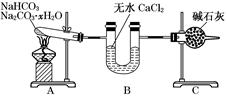
下列关于Na2CO3和NaHCO3的叙述中,正确的是
| A.NaHCO3的俗称是苏打 |
| B.Na2CO3溶液显碱性,说明Na2CO3属于碱 |
| C.相同条件下,在水中碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| D.向Na2CO3和NaHCO3固体中分别滴加等浓度的盐酸,后者反应速率快 |
D
试题分析:碳酸钠俗称苏大,碳酸氢钠俗称小苏打,A不正确;Na2CO3溶液显碱性,但Na2CO3属于盐,B不正确;相同条件下,在水中碳酸钠的溶解度大于碳酸氢钠的溶解度,C不正确;碳酸钠和盐酸反应是分两步进行的,所以向Na2CO3和NaHCO3固体中分别滴加等浓度的盐酸,后者反应速率快,D正确,答案选D。
点评:该题是高考中的常见考点,属于中等难度的试题。试题针对性强,紧扣教材基础知识,有利于培养分析、归纳和总结问题的能力。该题的关键是熟练记住二者的性质差异,然后结合题意灵活运用即可。

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目