��Ŀ����
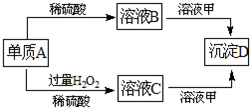 ��2011?Ϋ��ģ�⣩A��B��C��D�ͼ�������ת����ϵ����֪���ʼ��Ƕ�����Ԫ����ɵ��Σ�����ij������Һ����Ч�ɷ֣�����D�������ᣮ��ش��������⣺
��2011?Ϋ��ģ�⣩A��B��C��D�ͼ�������ת����ϵ����֪���ʼ��Ƕ�����Ԫ����ɵ��Σ�����ij������Һ����Ч�ɷ֣�����D�������ᣮ��ش��������⣺��1�����A��Ԫ�������ڱ���λ�ڵ�
��
��
���ڵ���
��
�壮��2������C�������ӣ�������H+���IJ�����������
ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+����
ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+����
����3��Aת��ΪBʱ��ų���ɫ����E����298Kʱ1mol A��ȫ��Ӧ�ų�����QkJ����÷�Ӧ���Ȼ�ѧ����ʽΪ
Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol
Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol
����4����Aת��ΪCʱ������ų���д���÷�Ӧ�Ļ�ѧ����ʽ��
2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O
2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O
����5��д����ҺC����Һ��Ӧ�����ӷ���ʽ��
Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO
Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO
�����������ʼ��Ƕ�����Ԫ����ɵ��Σ�����ij������Һ����Ч�ɷ֣���ΪNaClO������A��ϡ���ᷴӦ����B��AΪ������BΪ�����Σ�����A��ϡ���ᡢ�������ⷴӦ����C����֪����AΪ��۽�������AΪFe��BΪFeSO4��CΪFe2��SO4��3��FeSO4��Һ�����������Һ������������Ӧ��ˮ�ⷴӦ������Fe��OH��3��Fe2��SO4��3��Һ�����������Һ����ˮ�ⷴӦ������Fe��OH��3��DΪFe��OH��3������ת����ϵ��
����⣺���ʼ��Ƕ�����Ԫ����ɵ��Σ�����ij������Һ����Ч�ɷ֣���ΪNaClO������A��ϡ���ᷴӦ����B��AΪ������BΪ�����Σ�����A��ϡ���ᡢ�������ⷴӦ����C����֪����AΪ��۽�������AΪFe��BΪFeSO4��CΪFe2��SO4��3��FeSO4��Һ�����������Һ������������Ӧ��ˮ�ⷴӦ������Fe��OH��3��Fe2��SO4��3��Һ�����������Һ����ˮ�ⷴӦ������Fe��OH��3��DΪFe��OH��3��
��1��������������֪��AΪFe��Ϊ26��Ԫ�أ������ڱ���λ�ڵ������ڵڢ��壻
�ʴ�Ϊ���ġ�����
��2��CΪFe2��SO4��3������Fe3+�����ǣ�ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+���ӣ�
�ʴ�Ϊ��ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+���ӣ�
��3����298Kʱ1molFe��������ȫ��Ӧ���������������������ų�����QkJ����÷�Ӧ���Ȼ�ѧ����ʽΪ��Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol��
�ʴ�Ϊ��Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol��
��4������ϡ���ᡢ�������ⷴӦ������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ��2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O��
�ʴ�Ϊ��2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O��
��5��Fe2��SO4��3��Һ�����������Һ����ˮ�ⷴӦ����Fe��OH��3����Ӧ�����ӷ���ʽΪ��Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO��
�ʴ�Ϊ��Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO��
��1��������������֪��AΪFe��Ϊ26��Ԫ�أ������ڱ���λ�ڵ������ڵڢ��壻
�ʴ�Ϊ���ġ�����
��2��CΪFe2��SO4��3������Fe3+�����ǣ�ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+���ӣ�
�ʴ�Ϊ��ȡ����C��Һ���Թ��У�����KSCN��Һ����Һ�Ժ�ɫ��˵��C����Fe3+���ӣ�
��3����298Kʱ1molFe��������ȫ��Ӧ���������������������ų�����QkJ����÷�Ӧ���Ȼ�ѧ����ʽΪ��Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol��
�ʴ�Ϊ��Fe��s��+2H+ ��aq��=Fe2+��aq��+H2��g������H=-QkJ/mol��
��4������ϡ���ᡢ�������ⷴӦ������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ��2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O��
�ʴ�Ϊ��2Fe+3H2O2+3H2SO4=Fe2��SO4��3+6H2O��
��5��Fe2��SO4��3��Һ�����������Һ����ˮ�ⷴӦ����Fe��OH��3����Ӧ�����ӷ���ʽΪ��Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO��
�ʴ�Ϊ��Fe3++3ClO-+3H2O=Fe��OH��3��+3HClO��
����������������ͼ�����ʽ����Fe��Cl��Ԫ�ص��ʼ��仯����֮����ת����ϵ����������������ѧ�������д������
�����м��Ƕ�����Ԫ����ɵ�������ij������Һ����Ч�ɷ֣�����A�����ᷴӦ�ص�Ϊ����ͻ�ƿڣ�B��D��ѧ��İ��֪ʶ����Ҫ���������ԭ��Ӧ������ˮ��֪ʶ������������ѧ������������������ϸ�Ҫ���ѶȽϴ�
�����м��Ƕ�����Ԫ����ɵ�������ij������Һ����Ч�ɷ֣�����A�����ᷴӦ�ص�Ϊ����ͻ�ƿڣ�B��D��ѧ��İ��֪ʶ����Ҫ���������ԭ��Ӧ������ˮ��֪ʶ������������ѧ������������������ϸ�Ҫ���ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ