题目内容
【题目】某实验小组利用如图所示装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体,(图中夹持及尾气处理装置均已略去)回答下列问题:
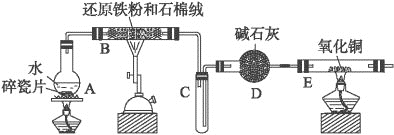
(1)装置B中发生反应的化学方程式是___;
(2)B、E两处酒精灯,必须后点燃的是___;
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3·6H2O晶体。
①欲检验溶液里含有Fe3+,选用的试剂为__,现象是__。
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因___。
【答案】3Fe+4H2O(g)![]() Fe3O4+4H2 E KSCN溶液 向溶液里滴加KSCN溶液,溶液变血红色 Fe+2Fe3+=3Fe2+
Fe3O4+4H2 E KSCN溶液 向溶液里滴加KSCN溶液,溶液变血红色 Fe+2Fe3+=3Fe2+
【解析】
Fe与水蒸气反应生成Fe3O4和H2;碱石灰能干燥气体;
(2)首先产生还原性气体,赶尽E装置中的空气,然后点燃E处装置中的酒精灯;
(3)①Fe3+的检验方法是:取少量滤液,滴入几滴硫氰化钾溶液,观察溶液是否变红色;
②向体系中加入铁粉,如果铁粉不溶解,说明不存在Fe3+;
(1)Fe与水蒸气反应生成Fe3O4和H2,反应的化学方程式是3Fe+4H2O(g)![]() Fe3O4+4H2,
Fe3O4+4H2,
故答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)首先产生还原性气体,赶尽E装置中的空气,然后点燃E处装置中的酒精灯,故选E,
故答案为:E;
(3)①Fe3+的检验方法是:取少量滤液,滴入几滴硫氰化钾溶液,观察溶液是否变红色,
故答案为:KSCN溶液;向溶液里滴加KSCN溶液,溶液变血红色;
②向体系中加入铁粉,如果铁粉不溶解,说明不存在Fe3+,所以离子反应方程式为:Fe+2Fe3+=3Fe2+,
故答案为:Fe+2Fe3+=3Fe2+。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】利用如图所示装置进行下列实验,不能达到相应实验目的的是( )
选项 | ① | ② | ③ | 实验目的 |
|
A | 稀硫酸 | Na2S | AgCl的浊液 | 验证Ag2S比AgCl难溶 | |
B | 浓硝酸 | Cu片 | NaOH溶液 | 探究浓硝酸具有氧化性 | |
C | 硫酸 | Na2SO3 | 酸性KMnO4溶液 | 探究SO2具有还原性 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 验证酸性:硝酸>碳酸>硅酸 |
A.AB.BC.CD.D