题目内容
17.等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )①它们所含的分子数目之比为1:1
②它们所含的O原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为1:1
⑥它们的质量之比为1:1.
| A. | ①和④ | B. | ②和③ | C. | ④和⑤ | D. | ①②③④ |
分析 ①由N=nNA可知,分子数目之比等于物质的量之比;
②CO和CO2分子分别含有1个、2个O原子;
③每个CO含有2个原子,每个CO2含有3个原子;
④CO和CO2分子均含有1个C原子;
⑤每个CO含有6+8=14个电子,每个CO2含有6+2×8=22个电子;
⑥根据m=nM计算二者质量之比.
解答 解:①由N=nNA可知:相等物质的量的CO和CO2所含的分子数目之比为1:1,故①正确;
②由CO和CO2的分子组成可知,它们所含的氧原子数目之比为1:2,故②正确;
③每个CO含有2个原子,每个CO2含有3个原子,相等物质的量的CO和CO2所含的原子总数目之比为2:3,故③正确;
④CO和CO2分子均含有1个C原子,它们所含的C原子数目之比等于分子数目之比,含有碳原子数目之比为1:1,故④正确;
⑤每个CO含有6+8=14个电子,每个CO2含有6+2×8=22个电子,相等物质的量的CO和CO2所含的电子数目之比为14;22=7:11,故⑤错误;
⑥根据m=nM可知,相等物质的量的CO和CO2的质量之比为28g/mol:44g/mol=7:11,故⑥错误,
故选:D.
点评 本题考查物质的量的相关计算,涉及微粒数目进行,侧重于分子组成和原子结构的考查,题目难度不大.

练习册系列答案
相关题目
7.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 活泼金属做原电池的负极 | Mg-Al-NaOH构成的原电池Mg做负极 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
| A. | A | B. | B | C. | C | D. | D |
12.选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是( )
| A. | 不溶于水,且必须易与碘发生化学反应 | |
| B. | 不溶于水,不与碘发生化学反应且比水更易溶解碘 | |
| C. | 不溶于水,且必须比水密度大 | |
| D. | 不溶于水,且必须比水密度小 |
2.下列化合物中既含离子键又含共价键的是( )
| A. | CO2 | B. | H2O | C. | NaOH | D. | BaCl2 |
9.下列实验现象预测不正确的是( )


| A. | 实验Ⅰ:振荡后静置,上层溶液变为无色 | |
| B. | 实验Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 | |
| C. | 实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 实验Ⅳ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
7.化学在生产和生活中有着重要的应用.下列叙述正确的是( )
| A. | 味觉上具有酸味的食物就是酸性食物 | |
| B. | Fe3O4俗称铁红,常做红色油漆和涂料 | |
| C. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| D. | “地沟油”禁止食用,但处理后可用来制肥皂和生物柴油 |
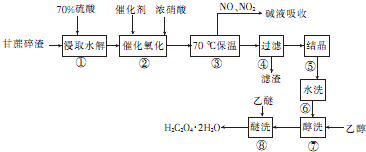
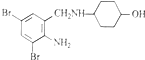 ,不考虑立体异构)是临床上使用广泛的祛痰药.下图所示是其多条合成路线中的一条(反应试剂和反应条件均未标出).
,不考虑立体异构)是临床上使用广泛的祛痰药.下图所示是其多条合成路线中的一条(反应试剂和反应条件均未标出).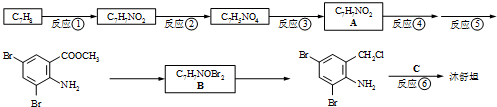
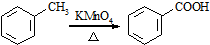 ,(2)反应③为还原反应
,(2)反应③为还原反应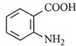 B
B 试剂C
试剂C
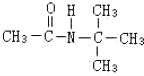 、
、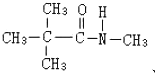 .
.