题目内容
18.用铝制易拉罐收集满CO2,加入过量NaOH浓溶液,立即把口封闭.发现易拉罐“咔咔”作响并变瘪了,过了一会儿,易拉罐又作响并鼓起来,下列有关判断正确的是( )| A. | 导致易拉罐变瘪的离子反应是CO2+OH-═HCO3 | |
| B. | 导致易拉罐又鼓起来的原因是:又生成了二氧化碳气体使得压强增大 | |
| C. | 上述过程中共发生了三个化学反应,且反应结束后的溶液呈碱性 | |
| D. | 若将CO2换为 NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
分析 易拉罐变瘪发生CO2+2OH-═CO32-+H2O,气体的压强变小;过一会儿后,易拉罐又会作响并鼓起来,发生2Al+2OH-+2H2O═2AlO2-+3H2↑,气体压强增大,以此来解答.
解答 解:A.气体与碱反应,导致易拉罐变瘪,反应为CO2+2OH-═CO32-+H2O,故A错误;
B.易拉罐又会作响并鼓起来,发生2Al+2OH-+2H2O═2AlO2-+3H2↑,气体压强增大,故B错误;
C.上述过程共发生CO2+2OH-═CO32-+H2O、2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2NaOH=2NaAlO2+H2O反应,反应后溶液显碱性,故C正确;
D.将CO2换为NH3,浓NaOH溶液换为水,只发生氨气与水反应,则易拉罐也会出现变瘪的现象,故D错误;
故选C.
点评 本题考查Al的化学性质及离子反应,为高频考点,明确发生的化学反应是解答本题的关键,题目难度不大,选项C为解答的难点,侧重分析与知识应用能力的考查.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
8.下列有关环境、健康及能源的叙述中,不正确的是( )
| A. | 氮的氧化物是光化学烟雾的主要污染物,二氧化碳是温室效应的主要污染物,所以它们的含 量是空气质量报告的主要项目 | |
| B. | PM2.5表面积大,能吸附大量的有毒有害的物质,对人的肺功能造成很大伤害 | |
| C. | 聚乙烯是生产食品保鲜膜、塑料水杯等生活用品的主要材料,不能用聚氯乙烯替代 | |
| D. | 利用催化转化装置可以将汽车尾气中的NOx、CO等有害气体转化为N2、CO2等无害气体 |
9.下列说法不正确的是( )
| A. | 乙烯能使酸性高锰酸钾溶液褪色,发生了氧化反应 | |
| B. | 苯在一定条件下能与浓硝酸反应得到硝基苯,发生了取代反应 | |
| C. | 邻二氯苯不存在同分异构体说明了苯不存在单双键交替的结构 | |
| D. | 1mol甲烷和1mol氯气在光照条件下发生反应,产物只有CH3Cl和HCl |
13.氮的化合物既是一种资源,也会给环境造成危害.
I.氨气是一种重要的化工原料.
(1)NH3与CO2在120°C,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)?(NH2)2CO(s)+H2O(g),△H=-x KJ/mol (x>0),其他相关数据如表:
则表中z(用x a b d表示)的大小为x-d+b+2a.
(2)120℃时,在2L密闭反应容器中充入3mol CO2与NH3的混合气体,混合气体中NH3的体积分数随反应时间变化关系如图2所示,该反应到达平衡时CO2的平均反应速率为0.00417mol/(L•s),此温度时的平衡常数为8.

下列能使正反应的化学反应速率加快的措施有②③.
①及时分离出尿素 ②升高温度 ③向密闭定容容器中再充入CO2 ④降低温度
Ⅱ.氮的氧化物会污染环境.目前,硝酸厂尾气治理可采用NH3与于NO在催化剂存在的条件下作用,将污染物转化为无污染的物质.某研究小组拟验证NO能被氨气还原并计算其转化率(已知浓硫酸在常温下不氧化NO气体).
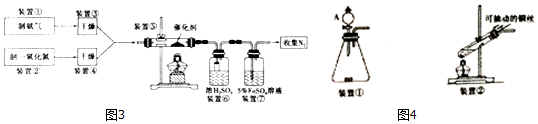
(l)写出装置⑤中反应的化学方程式4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O.
(2)装置①和装置②如图4,仪器A的名称为分液漏斗,其中盛放的药品名称为浓氨水.
装置②中,先在试管中加入2-3 粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用是产生CO2,排出装置中的空气,防止NO被氧化.
(3)装置⑥中,小段玻璃管的作用是防倒吸;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,可观察到的实验现象是溶液变浑浊.
I.氨气是一种重要的化工原料.
(1)NH3与CO2在120°C,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)?(NH2)2CO(s)+H2O(g),△H=-x KJ/mol (x>0),其他相关数据如表:
| 物质 | NH3(g) | CO2(g) | CO(NH2)2(s) | H2O(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/KJ | a | b | z | d |
(2)120℃时,在2L密闭反应容器中充入3mol CO2与NH3的混合气体,混合气体中NH3的体积分数随反应时间变化关系如图2所示,该反应到达平衡时CO2的平均反应速率为0.00417mol/(L•s),此温度时的平衡常数为8.

下列能使正反应的化学反应速率加快的措施有②③.
①及时分离出尿素 ②升高温度 ③向密闭定容容器中再充入CO2 ④降低温度
Ⅱ.氮的氧化物会污染环境.目前,硝酸厂尾气治理可采用NH3与于NO在催化剂存在的条件下作用,将污染物转化为无污染的物质.某研究小组拟验证NO能被氨气还原并计算其转化率(已知浓硫酸在常温下不氧化NO气体).

(l)写出装置⑤中反应的化学方程式4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O.
(2)装置①和装置②如图4,仪器A的名称为分液漏斗,其中盛放的药品名称为浓氨水.
装置②中,先在试管中加入2-3 粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用是产生CO2,排出装置中的空气,防止NO被氧化.
(3)装置⑥中,小段玻璃管的作用是防倒吸;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,可观察到的实验现象是溶液变浑浊.
3.化学与生产、生活、环境等密切相关.下列说法正确的是( )
| A. | 开发氟氯代烷制冷剂,有利于保护臭氧层 | |
| B. | 绿色食品就是不使用农药,不含任何化学物质的食品 | |
| C. | 推广使用煤液化技术,可减少二氧化碳温室气体的排放 | |
| D. | 使用可降解的无毒聚乳酸塑料代替乙烯作食品包装袋,可减少白色污染 |
10.下列有关化学反应速率的说法中正确的是( )
| A. | 实验室制氢气时,加入少量NaNO3固体,不影响反应速率 | |
| B. | 锌片分别与c(H+)相等的醋酸、硫酸反应,平均反应速率相等 | |
| C. | 升高温度后,吸热反应的速率加快,放热反应的速率减慢 | |
| D. | 纳米铁粉在空气中自燃,是因为纳米铁粉的表面积大 |
7.下列各组有机物无论以何种比例混合,混合物中碳、氢比例不变的是( )
| A. | CH4和C2H4 | B. | C2H6和C2H4 | C. | C6H6和C2H4 | D. | C6H6和C2H2 |
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O
+3H2O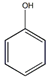 +3Br2→
+3Br2→ ↓+3HBr
↓+3HBr