题目内容
(10分)根据下列变化关系:

请填空:
(1)A物质的名称_____ 。B溶液为____________.作用为_________________________
(2)写出④、⑥两步反应的化学方程式,在( )号中标明反应类型。
④ ________________________________________( )
⑥_______________________________________________( )
【答案】
(1)葡萄糖(1分) NaOH溶液(1分) 中和稀H2SO4(2分)
(2)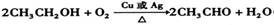 (氧化反应)
(氧化反应)
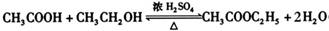 (酯化或取代反应)
(酯化或取代反应)
(方程式2分,类型1分)
【解析】淀粉在催化剂的作用下水解生成葡萄糖,即A是葡萄糖。葡萄糖在酶的作用下分解产生乙醇,所以D是乙醇,乙醇发生催化氧化生成乙醛,乙醛钡氧化则生成乙酸。乙酸和乙醇发生酯化反应生成乙酸乙酯,即E是乙酸乙酯。淀粉的水解产物要和新制的氢氧化铜悬浊液反应,需要在碱性条件下,所以在加入氢氧化铜之前,要先加入氢氧化钠,中和硫酸,即B是氢氧化钠,C是氢氧化铜。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
(10分)在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是 ,所发生反应的化学方程式是 。
(2)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是
① ,② 。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是
| A.有气体生成 | B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 | D.溶液变浑浊 |
在反应过程中,若生成标准状况下224mL的H2,则转移的电子的物质的量为 。
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是
。

 的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
 CH3OH(g)
CH3OH(g)