题目内容
300mLkOH溶液中缓慢通入一定量的SO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
(1)由于SO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。
(2)若通入SO2气体2.24L(标准状况下),得到13.9g白色固体。请通过计算确定此白色固体是由哪些物质组成的,其质量各为多少?所用的KOH溶液的物质的量浓度为多少?
(1)四种可能:①K2SO3、KOH;②K2SO3;③K2SO3、KHSO3;④KHSO3。
(2)白色固体是KHSO3、K2SO3,KHSO3为6g,K2SO3为7.9g;KOH浓度为0.500mol·L-1。
解析:
根据有关反应:2KOH+SO2 ![]() K2SO3+H2O,KOH+SO2
K2SO3+H2O,KOH+SO2 ![]() KHSO3分析:若KOH与SO2按物质的量之比为2∶1恰好反应,则生成物为K2SO3;若KOH过量,则生成物为K2SO3,还有剩余的KOH;若KOH与SO2按物质的量之比为1∶1恰好反应,则生成物为KHSO3;若KOH与SO2的物质的量之比介于1∶1与2∶1之间,则生成物既有K2SO3,又有KHSO3。因此第(2)小题按极限值讨论,若全部为K2SO3:0.1mol×158g·mol-1=15.8g>13.9g;若全部为KHSO3:0.1mol×120g·mol-1=12.0g<13.9g。综上所述,此白色固体为KHSO3和K2SO3的混合物。设混合物中含K2SO3的物质的量为x,KHSO3 的物质的量为y,据题意列二元一次方程组如下:
KHSO3分析:若KOH与SO2按物质的量之比为2∶1恰好反应,则生成物为K2SO3;若KOH过量,则生成物为K2SO3,还有剩余的KOH;若KOH与SO2按物质的量之比为1∶1恰好反应,则生成物为KHSO3;若KOH与SO2的物质的量之比介于1∶1与2∶1之间,则生成物既有K2SO3,又有KHSO3。因此第(2)小题按极限值讨论,若全部为K2SO3:0.1mol×158g·mol-1=15.8g>13.9g;若全部为KHSO3:0.1mol×120g·mol-1=12.0g<13.9g。综上所述,此白色固体为KHSO3和K2SO3的混合物。设混合物中含K2SO3的物质的量为x,KHSO3 的物质的量为y,据题意列二元一次方程组如下:
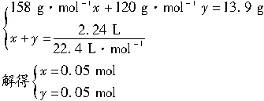
c(KOH)=![]() =0.500mol·L-1
=0.500mol·L-1
m(KHSO3)=120g·mol-1×0.05mol=6g
m(K2SO3)=158g·mol-1×0.05mol=7.9g。

(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试写出所有可能的组成,填入下表,可以不填满.
| 可能情况 | ① | ② | ③ | ④ | ⑤ |
| 组成物质 |
向300mLKOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.请回答下列问题:(直接填空,不写过程)
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试写出所有可能的组成,填入下表,可以不填满.
| 可能情况 | ① | ② | ③ | ④ | ⑤ |
| 组成物质 |