题目内容
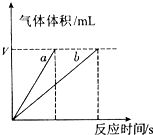 为了研究外界条件对H2O2分解反应速率的影响,某同学在四支试管中分别加入3mLH2O2溶液,并测量收集VmL气体所需的时间,实验记录如下:
为了研究外界条件对H2O2分解反应速率的影响,某同学在四支试管中分别加入3mLH2O2溶液,并测量收集VmL气体所需的时间,实验记录如下:| 实验序号 | H2O2溶液浓度 | H2O2溶液温度 | 催化剂 | 所用时间 |
| ① | 5% | 20℃ | 2滴1mol/LFeCl3 | t1 |
| ② | 5% | 40℃ | 2滴1mol/LFeCl3 | t2 |
| ③ | 10% | 20℃ | 2滴1mol/LFeCl3 | t3 |
| ④ | 5% | 20℃ | 不使用 | t4 |
(1)过氧化氢分解的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(2)实验①②是研究
温度
温度
对反应速率的影响.(3)实验测得t1>t3,原因是
其他条件相同时,实验③的反应物浓度大于实验①的反应物浓度,所以实验③的反应速率大于实验①的反应速率
其他条件相同时,实验③的反应物浓度大于实验①的反应物浓度,所以实验③的反应速率大于实验①的反应速率
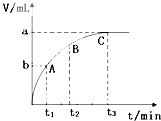
.(4)实验①④的测定过程如图,曲线a对应的实验序号是
①
①
(填“①”或“④”).分析:(1)在氯化铁作催化剂条件下,双氧水分解生成氧气和水;
(2)实验①②的不同点确定影响因素;
(3)根据①③的不同点分析,反应物浓度与反应速率成正比;
(4)催化剂能加快反应速率,缩短反应时间.
(2)实验①②的不同点确定影响因素;
(3)根据①③的不同点分析,反应物浓度与反应速率成正比;
(4)催化剂能加快反应速率,缩短反应时间.
解答:解:(1)在氯化铁作催化剂条件下,双氧水分解生成氧气和水,反应方程式为:2H2O2
2H2O+O2↑,
故答案为:2H2O2
2H2O+O2↑;
(2)实验①②的不同点是温度,所以实验①②是研究温度对反应速率的影响,故答案为:温度;
(3)实验①③的不同点是反应物浓度,实验测得t1>t3,反应时间越长,反应速率越小,所以实验①的速率小于实验③,比较实验①③知,在其它条件相同时,反应物浓度越大,其反应速率越快,
故答案为:其他条件相同时,实验③的反应物浓度大于实验①的反应物浓度,所以实验③的反应速率大于实验①的反应速率;
(4)反应①有催化剂,反应④没有催化剂,氯化铁能加快双氧水的分解速率,所以收集相同体积的气体,有催化剂的使用时间段,没有催化剂的时间长,根据图象知曲线a对应的实验序号是①,
故答案为:①.
| ||
故答案为:2H2O2
| ||
(2)实验①②的不同点是温度,所以实验①②是研究温度对反应速率的影响,故答案为:温度;
(3)实验①③的不同点是反应物浓度,实验测得t1>t3,反应时间越长,反应速率越小,所以实验①的速率小于实验③,比较实验①③知,在其它条件相同时,反应物浓度越大,其反应速率越快,
故答案为:其他条件相同时,实验③的反应物浓度大于实验①的反应物浓度,所以实验③的反应速率大于实验①的反应速率;
(4)反应①有催化剂,反应④没有催化剂,氯化铁能加快双氧水的分解速率,所以收集相同体积的气体,有催化剂的使用时间段,没有催化剂的时间长,根据图象知曲线a对应的实验序号是①,
故答案为:①.
点评:本题考查了探究外界条件对反应速率的影响,难度不大,注意探究影响因素时,其它因素必须完全相同,只有一个条件不同才能得出结论,难度中等.

练习册系列答案
相关题目
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]2KMnO4 + 5H2C2O4 + 3H2SO4 === K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
[实验内容及记录]
|
实验编号 |
室温下,试管中所加试剂及其用量 / mL |
室温下溶液颜色褪至无色所需时间 / min |
|||
|
0.6 mol/L H2C2O4溶液 |
H2O |
0.2mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
||
|
1 |
3.0 |
2.0 |
3.0 |
2.0 |
4.0 |
|
2 |
3.0 |
3.0 |
2.0 |
2.0 |
5.2 |
|
3 |
3.0 |
4.0 |
1.0 |
2.0 |
6.4 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:υ(KMnO4) = 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
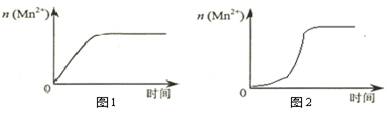
①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
|
实验编号 |
室温下,试管中所加试剂及其用量 / mL |
再向试管中加入少量固体 |
室温下溶液颜色褪至无色所需时间 / min |
|||
|
0.6 mol/L H2C2O4溶液 |
H2O |
0.2 mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
|||
|
4 |
3.0 |
2.0 |
3.0 |
2.0 |
|
t |
③若该小组同学提出的假设成立,应观察到的现象是 。
 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.