题目内容
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
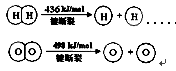
下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
D

练习册系列答案
相关题目
请回答下列问题:
(1)在一定温度下,下列叙述是可逆反应A(g)+3B(g) 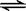 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amol B;
③A、B 、C的浓度不再变化;
、C的浓度不再变化;
④A、B、C的分子数目比为1:3:2 ;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间消耗amol A,同时生成3amol B;
⑧单位时间内生成a mol C,同时生成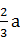 mol B
mol B
(2)在稀氨水中存在下述电离平衡NH3+H2O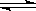 NH3 ·H2O
NH3 ·H2O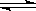 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
| 加入的物质 | 少量NH4Cl | 少量KOH溶液 |
| c(OH-)的变化 | ||
| 平衡移动方向 |
下述实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积的盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 向溶液中加入淀粉 |
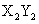
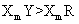
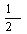 N2(g) + CO2(g);△H=-373.2 kJ/mol ,达到平衡后,为提高该反应的速率和NO的转化率,采取的措施正确的是
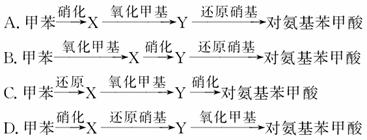
N2(g) + CO2(g);△H=-373.2 kJ/mol ,达到平衡后,为提高该反应的速率和NO的转化率,采取的措施正确的是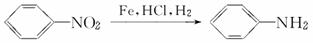 ,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是
,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是