题目内容
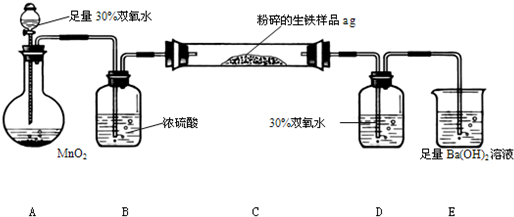
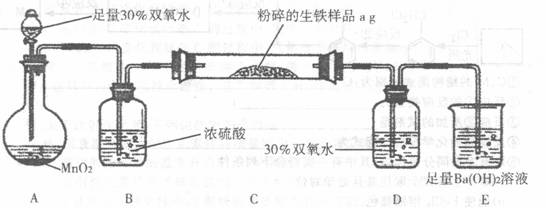
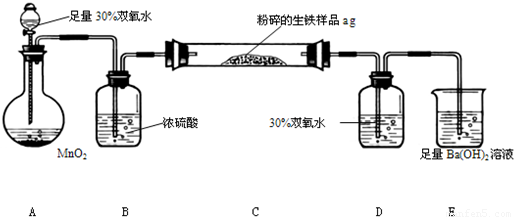
生铁中除铁外,还含有其他元素,如碳元素和硫元素。其中碳主要以碳化铁的形态存在,它使生铁性能坚硬而脆,所以生铁的用途不大,一般用做炼钢的原料。某兴趣小组设计按下图所示的实验装置,测定生铁中的含碳量。

A??????????? B????????????????? C????????????????? D???????? E
请回答下列问题:
(1)硫在生铁中是有害元素,它使生铁产生热脆性。硫元素在生铁中最有可能存在的价态是???????????
A、-2?? ? B、0? ?? C、+4?? ?? D、+6
(2)写出在烧杯E中发生反应的离子方程式:???????????????????????????? ;
(3)D中30% 双氧水的作用是???????????????????????????????????????????????? ;若无此装置,所测定的含碳量将??????? (填“偏高”、“偏低”或“不影响”)
(4)反应完成后,欲验证生铁含有硫元素,你所设计的实验方案是(写出实验步骤、现象)???????????????????????????????????????????????????? ;
(5)待C管的样品充分反应后,测得E中生成的沉淀为bg,请计算出生铁中的含碳量为???????????? ;
(6)实验过程中,该兴趣小组应注意的安全问题是???????????????????? 。(任写一种)
(1)A (2分)
(2)CO2+Ba2++2OH-= BaCO3↓+H2O(3分)
(3)吸收SO2气体 (2分)??? 偏高 (2分)
(4)取少量D瓶溶液于试管中,滴加盐酸酸化的BaCl2溶液,若出现白色沉淀,说明生铁中含有硫元素。(2分)
(5) ×100%(2分)
×100%(2分)
(6)浓硫酸有腐蚀性,使用时要小心;加热时要使二通管均匀受热等(其他合理答案也给分)(2分)
【解析】
试题分析:(1)铁的化合价一定为正价,而碳的非金属小于硫的非金属性,因此S一定显示负价,故A项正确。
(2)二氧化碳与氢氧化钡反应生成碳酸钡与水,反应离子方程式为:CO2+Ba2++2OH-=BaCO3↓+H2O。
(3)如果没有双氧水的氧化,二氧化硫也会与氢氧化钡反应生成白色沉淀,使碳的百分含量偏高,故D中30%双氧水的作用是吸收SO2气体;若无此装置,所测定的含碳量将偏高。
(4)反应完成红叶,S元素转化为SO42?,用盐酸酸化的BaCl2溶液检验,所以实验方案是:取少量D瓶溶液于试管中,滴加盐酸酸化的BaCl2溶液,若出现白色沉淀,说明生铁中含有硫元素。
(5)若E中得到bg碳酸钡,根据碳元素守恒可知碳酸钡的物质的量与二氧化碳的物质的量相等,故生铁中碳的质量为:bg÷197g/mol×12g/mol=12b/197g,所以生铁中的含碳量为:12b/197g÷ag×100%= ×100%
×100%
(6)实验过程中应注意的安全问题有:浓硫酸有腐蚀性,使用时要小心;加热时要使二通管均匀受热等。
考点:本题考查对实验方案设计与装置的理解、实验基本操作、离子方程式的书写、化学计算。

 智能训练练测考系列答案
智能训练练测考系列答案