题目内容
下列无色溶液中的离子能大量共存的是
| A.K+、Na+、MnO4-、SO42- | B.H+、K+、NO3-、SO32- |
| C.Na+、Ba2+、Cl-、Br- | D.Fe3+、NH4+、SCN-、HCO3- |
C
解析试题分析:大量存在高锰酸根离子的溶液呈紫红色,无色溶液中不能大量存在高锰酸根离子,故A错误;氢离子与亚硫酸根离子能反应生成亚硫酸,硝酸根离子在酸性条件下可以将亚硫酸根离子氧化为硫酸根离子,故B错误;该组离子均无色,相互之间不能生成难溶物、难电离物、易挥发物,也不能发生氧化还原反应,故C正确;大量存在铁离子的溶液呈黄色,无色溶液中不能大量存在铁离子,铁离子遇硫氰酸根离子时溶液变红,铁离子与碳酸氢根离子能发生双水解反应,生成氢氧化铁沉淀和二氧化碳气体,故D正确。
考点:考查离子共存。

练习册系列答案
相关题目
下列离子方程式正确的是
| A.用氢氧化钠溶液除去铝片表而上的氧化膜:Al3++4OH-=AlO2-+2H2O |
| B.在含3.2amolHNO3的稀溶液中,加入amol铁粉:5Fe+4NO3-+16H+=3Fe2++2Fe3++4NO↑+8H2O |
| C.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D.过氧化氢能使酸性KMnO4溶液褪色:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O |
下列离子方程式正确的是
| A.氨水吸收足量的SO2气体:OH-+SO2=HSO3- |
| B.稀硝酸中加入过量铁粉: Fe + 4H++ NO3-=Fe3++ NO↑ + 2H2O |
| C.用NaOH溶液吸收废气中氮氧化物:NO+NO2+OH-=NO2-+H2O |
D.苯酚钠溶液中通入少量CO2: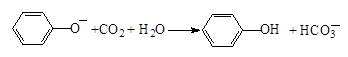 |
下列离子方程式正确的是
| A.氢氧化镁与稀盐酸反应:H+ + OH-=H2O |
| B.AlCl3溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ |
| C.铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D.次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
下列溶液中,各组离子一定能大量共存的是
| A.能使石蕊试液呈蓝色的溶液:Na+、I-、Cl-、NO3- |
| B.含大量Fe3+的溶液:NH4+、Na+、Cl-、SCN- |
| C.能与Al反应生成H2的溶液:Ca2+、NH4+、HCO3-、Cl- |
| D.水电离出的c(H+)=1×10-14mol/L的溶液:K+、AlO2-、Br-、Cl- |
在溶液中能大量共存的一组离子或分子是
| A.K+ 、Al3+、SO42—、NH3·H2O | B.NH4+、H+、NO3—、HCO3— |
C.Na+ 、CH3COO—、CO32—、OH— | D.Na+、K+、SO32—、Cl2 |
在酸性溶液中,下列各组离子能大量共存且溶液为无色透明的是
| A.Na+、K+、OH-、Cl- | B.Na+、Cu2+、SO42-、NO3- |
| C.Mg2+、Na+、SO42-、Cl- | D.K+、Na+、NO3-、CO32- |
钠与水反应的离子方程式正确的是( )
| A.2Na+3H+=2Na++H2↑ |
| B.Na+H2O=Na++OH-+H2↑ |
| C.2Na+2H2O=2Na++2OH-+H2↑ |
| D.2Na+2H2O=2Na++O2↑+2H2↑ |
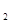 溶液,当Al3+恰好全部沉淀时:
溶液,当Al3+恰好全部沉淀时: