题目内容
(每格2分,共12分)写出下列反应的离子方程式:
(1)过氧化钠溶于水 ;
(2)苏打溶液中滴入少量盐酸 ;
(3)实验室制Cl2 ;
(4)Al和NaOH溶液反应 ;
(5)向NaHSO4溶液中逐滴加入Ba (OH)2溶液至溶液呈中性 ;在以上中性溶液中,继续滴加Ba(OH)2溶液 。
(12分)(1) 2Na2O2+ 2H2O= 4Na++OH- +O2↑
(2) CO32-+H+= HCO3-
(3) 4H++2Cl-+MnO2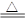 Mn2+ +Cl2+2H2O
Mn2+ +Cl2+2H2O
(4) 2Al + 2OH- + 2H2O =2AlO2- + 3H2
(5)2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O; Ba2++ SO42- =BaSO4↓
每格2分,共14分。
【解析】
试题分析:(1)过氧化钠溶于水的化学方程式为2Na2O2+
2H2O= 4NaOH+O2↑,只有NaOH可以拆开,其余不能拆开,则离子方程式为2Na2O2+ 2H2O= 4Na++OH-
+O2↑;(2)因为少量盐酸,所以只能生成碳酸氢钠,不能生成二氧化碳,CO32-+H+= HCO3-;(3)实验室制Cl2一般用浓盐酸和二氧化锰,需要加热,4H++2Cl-+MnO2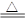 Mn2+ +Cl2+2H2O;(4)Al和NaOH溶液反应生成偏铝酸钠与氢气,要注意有水参与反应,2Al + 2OH- + 2H2O =2AlO2-
+ 3H2;(5)向NaHSO4溶液中逐滴加入Ba (OH)2溶液至溶液呈中性则两者的比例是2:1,所以离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,继续滴加Ba(OH)2溶液酸已经反应完成,只有多余的硫酸根离子与钡离子反应,Ba2++ SO42- =BaSO4↓。
Mn2+ +Cl2+2H2O;(4)Al和NaOH溶液反应生成偏铝酸钠与氢气,要注意有水参与反应,2Al + 2OH- + 2H2O =2AlO2-
+ 3H2;(5)向NaHSO4溶液中逐滴加入Ba (OH)2溶液至溶液呈中性则两者的比例是2:1,所以离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,继续滴加Ba(OH)2溶液酸已经反应完成,只有多余的硫酸根离子与钡离子反应,Ba2++ SO42- =BaSO4↓。
考点:考查离子方程式的书写。
点评:在书写离子方程式中,一般有写、拆、删、查四步,难点是哪些物质该拆,哪些物质不该拆开:强酸、强碱和可溶性盐要拆写成离子形式。难溶性物质或难电离的物质:难溶性盐、弱酸、弱碱、气体、单质、氧化物仍用化学式。

 阅读快车系列答案
阅读快车系列答案