题目内容
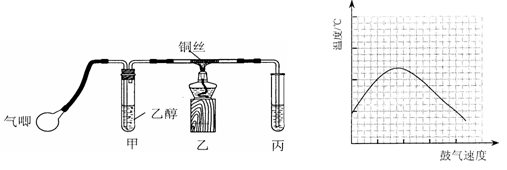
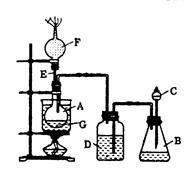
某课外活动小组利用如下左图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去。实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气。请填写下列空白:
(1)检验乙醛的试剂是 ;
(2)乙醇发生催化氧化的化学反应方程式为 ;
(3)实验时,常常将甲装置浸在70℃~80℃的水浴中,目的是 ___ ,由于装置设计上的缺陷,实验进行时可能会 _____ 。
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行。进一步研究表明,鼓气速度与反应体系的温度关系曲线如上右图所示。
试解释鼓气速度过快,反应体系温度反而下降的原因: ,该实验中“鼓气速度”这一变量你认为可用 来估量;
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色。该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。请你设计一个简单的实验,探究哪一种猜想正确?

(1)检验乙醛的试剂是 ;
| A.银氨溶液 | B.碳酸氢钠溶液 | C.新制氢氧化铜悬浊液 | D.氧化铜 |
(3)实验时,常常将甲装置浸在70℃~80℃的水浴中,目的是 ___ ,由于装置设计上的缺陷,实验进行时可能会 _____ 。
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行。进一步研究表明,鼓气速度与反应体系的温度关系曲线如上右图所示。
试解释鼓气速度过快,反应体系温度反而下降的原因: ,该实验中“鼓气速度”这一变量你认为可用 来估量;
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色。该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。请你设计一个简单的实验,探究哪一种猜想正确?
(1)A、C
(2)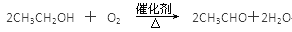
(3)使生成乙醇蒸气的速率加快且较均匀, 发生倒吸
(4)过量的气体将体系中的热量带走, 单位时间内甲中的气泡量
(5)用pH试纸检测溴水与褪色后溶液的酸碱性。若酸性明显增强,则猜想①正确;反之,猜想②正确(或其它合理方法)
(2)
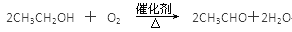
(3)使生成乙醇蒸气的速率加快且较均匀, 发生倒吸
(4)过量的气体将体系中的热量带走, 单位时间内甲中的气泡量
(5)用pH试纸检测溴水与褪色后溶液的酸碱性。若酸性明显增强,则猜想①正确;反之,猜想②正确(或其它合理方法)
(1)乙醛中含有醛基,可以通过银氨溶液或新制氢氧化铜悬浊液来检验。
(2)乙醇在催化剂的作用下可将羟基氧化生成醛基。
(3)乙醇的沸点是79℃,所以要获得乙醇蒸汽,需要将甲装置置于在70℃~80℃的水浴中。不论是乙醇还是乙醛均易溶于水,所以实验过程中可能发生倒吸现象。
(4)若鼓气过快,乙醇气体来不及反应将热量一同带走。因为鼓气时甲装置中会冒气泡,所以可以通过单位时间内甲中的气泡量来估量。
(5)若溴水把乙醛氧化生成乙酸,则溶液的酸性会明显的增强,若发生加成反应,则酸性会降低,所以可利用pH试纸来检验。
(2)乙醇在催化剂的作用下可将羟基氧化生成醛基。
(3)乙醇的沸点是79℃,所以要获得乙醇蒸汽,需要将甲装置置于在70℃~80℃的水浴中。不论是乙醇还是乙醛均易溶于水,所以实验过程中可能发生倒吸现象。
(4)若鼓气过快,乙醇气体来不及反应将热量一同带走。因为鼓气时甲装置中会冒气泡,所以可以通过单位时间内甲中的气泡量来估量。
(5)若溴水把乙醛氧化生成乙酸,则溶液的酸性会明显的增强,若发生加成反应,则酸性会降低,所以可利用pH试纸来检验。

练习册系列答案
相关题目
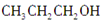
 __________。
__________。