题目内容
17.下列化合物的同分异构体数目为7种的是(不考虑立体异构)( )| A. | C6H10 | B. | C4H8 | C. | C4H10O | D. | C5H11Cl |
分析 判书写烷烃的氯代物的异构体方法:
(1)先确定烷烃的碳链异构,即烷烃的同分异构体.
(2)确定烷烃的对称中心,即找出等效的氢原子.
(3)根据先中心后外围的原则,将氯原子逐一去代替氢原子.
(4)对于多氯代烷的同分异构体,遵循先集中后分散的原则,先将几个氯原子集中取代同一碳原子上的氢,后分散去取代不同碳原子上的氢.
解答 解:A.C6H10的不饱和度为2,可以为二烯烃也可以为炔烃或环烯烃,
属于炔烃有C≡C-C-C-C-C、C-C≡C-C-C-C、C-C-C≡C-C-C、C≡C-C(-C)-C-C、C≡C-C-C(-C)-C、C-C≡C-C(-C)-C、C≡C-C(-C)2-C共7种;
属于二烯烃有C=CC=CCC、C=CCC=CC、C=CCCC=C、C=CC=C(C)2、C=C(C)C=CC、C=CC(C)=CC、C=CCC(C)=C、C=CC(C)C=C、CC=CC=CC共计9种,
属于环烯烃有32种:三元环:16种;四元环:11种;五元环:4种;六元环:1种,共48种,故A错误;
B.C4H8的有机物结构有:CH2=CHCH2CH3、CH2=C(CH3)2、CH3CH=CHCH3、 、
、 共5种,故B错误;
共5种,故B错误;
C.C4H10O,属于醇类的有CH3CH2CH2CH2OH、CH3CH2CH(CH3)OH、(CH3)2CHCH2OH、C(CH3)3OH等4种,C4H10O属于醚类的有CH3CH2CH2OCH3、CH3CH2OCH2CH3、(CH3)2CHOCH3等3,共7种,故C正确;
D.主链有5个碳原子的:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;
主链有4个碳原子的:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;
主链有3个碳原子的:CH2C(CH3)2CH2Cl,共有8种情况,故D错误,
故选C.
点评 本题主要考查的是同分异构体的书写,难度不大.

| A. |  | B. |  | C. |  | D. |  |
| A. | 2HgO $\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | 2A12O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | ||
| C. | H2+Na2O $\frac{\underline{\;高温\;}}{\;}$2Na+H2O | D. | 4 CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 |
| A. | $\frac{b-2c}{a}$ | B. | $\frac{2b-4c}{a}$ | C. | $\frac{2b-c}{a}$ | D. | $\frac{b-4c}{a}$ |
 某同学在实验室进行实验研究化学反应速率的影响因素.
某同学在实验室进行实验研究化学反应速率的影响因素.Ⅰ.下表是研究性学习小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2溶液制取150mL氧气所需的时间(单位:s)
浓 度 反应条件 | 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加 热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(2)该研究小组在设计方案时,考虑了浓度、温度、催化剂等反应条件对过氧化氢分解速率的影响.
(3)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?温度升高化学反应速率加快(或反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快).
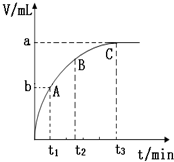
(4)某同学在10mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C.
(5)若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,反应的离子方程式为MnO2+2H++H2O2=Mn2++O2↑+2H2O.
Ⅱ.现提供下列实验用品研究化学反应速率的影响因素.
实验仪器:试管、烧杯、量筒、天平、秒表
实验药品:铝片、铝粉、0.5mol/L 盐酸、5mol/L 盐酸
①利用所提供实验用品,可研究的化学反应速率的影响因素是盐酸的浓度、铝的表面积,
为了便于观察,你建议记录的数据是反应开始到停止所用的时间.
②若要研究温度对化学反应速率的影响,还需用到的主要仪器是温度计.
| A. | 苯中的甲苯(溴水、分液) | B. | 乙醇中的乙酸(NaOH溶液,分液) | ||
| C. | 乙醇中的水(新制CaO,蒸馏) | D. | 乙酸乙酯中的乙酸(NaOH溶液,分液) |
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:MgO>NaCl>KCl | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
 .
. .
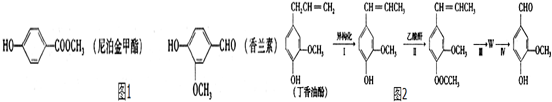
. 和ClCH2CH═CH2 合成丁香油酚的反应类型为取代反应.
和ClCH2CH═CH2 合成丁香油酚的反应类型为取代反应.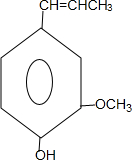 +CH3OCOCOCH3→
+CH3OCOCOCH3→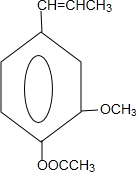 +CH3COOH.
+CH3COOH.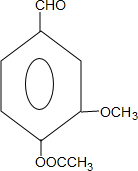 _.
_.