题目内容
下列有关电化学知识的说法,错误的是( )
| A、Fe、Cu长久地露置于空气中会发生电化腐蚀 |
| B、工业上冶炼Na、Mg、Al通常采用电解法 |
| C、电解精制铜,粗铜作阴极,发生氧化反应 |
| D、原电池工作时,电流一定是从正极流向负极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、Fe、Cu与其中的杂质能构成原电池;
B、活泼较强的金属用电解法冶炼;
C、电解精制铜,粗铜作阳极;
D、原电池工作时,电子从负极到正极,电流方向相反.
B、活泼较强的金属用电解法冶炼;
C、电解精制铜,粗铜作阳极;
D、原电池工作时,电子从负极到正极,电流方向相反.
解答:
解:A、Fe、Cu与其中的杂质能构成原电池,Fe、Cu作负极被腐蚀,所以Fe、Cu长久地露置于空气中会发生电化腐蚀,故A正确;
B、活泼较强的金属用电解法冶炼,如Na、Mg、Al不容易被其它还原剂还原,一般采用电解法冶炼,故B正确;
C、电解精制铜,粗铜作阳极失电子发生氧化反应,故C错误;
D、原电池中负极失电子,正极得电子,所以原电池工作时,电子从负极到正极,电流从正极流向负极,故D正确.
故选C.
B、活泼较强的金属用电解法冶炼,如Na、Mg、Al不容易被其它还原剂还原,一般采用电解法冶炼,故B正确;
C、电解精制铜,粗铜作阳极失电子发生氧化反应,故C错误;
D、原电池中负极失电子,正极得电子,所以原电池工作时,电子从负极到正极,电流从正极流向负极,故D正确.
故选C.
点评:本题综合考查原电池、电解池知识,侧重于电化学基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
室温下向一定量的稀氨水中加入水稀释后,下列说法正确的是( )
| A、因为稀释,溶液中所有离子的浓度均减小 | ||
B、溶液中
| ||
| C、NH3?H2O的电离程度增大,c(OH-)亦增大 | ||
| D、再加入与氨水等体积等浓度的盐酸,混合液pH=7 |
在氯化铁和盐酸的混合溶液中,已知c(Cl-)═a mol/L,pH═b<1,则溶液中c(Fe3+)为( )
A、
| ||
| B、(a-1×10-b) mol/L | ||
C、(a-
| ||
| D、上述答案都不正确 |
 如图表示反应2A(g)?B(g)+C(g)△H>0从平衡状态Ⅰ移到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化可能为( )
如图表示反应2A(g)?B(g)+C(g)△H>0从平衡状态Ⅰ移到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化可能为( )| A、加入催化剂 | B、加压 |
| C、增加A的浓度 | D、增加B的浓度 |
某温度下,对可逆反应2X(g)+Y(g)?3Z(g)+W(s)△H>0 的叙述正确的是( )
| A、加入少量W,逆反应速率增大,平衡向左移动 |
| B、增大压强,正反应速率增大,逆反应速率减小 |
| C、温度、体积不变,充入He气增大压强,反应速率会加快 |
| D、升高温度,混合气体的平均相对分子质量减小 |
短周期金属元素甲~戊在周期表中的相对位置如表所示,下面判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、原子半径:丙<丁<戊 |
| B、金属性:甲<丙 |
| C、氢氧化物碱性:丙<丁<戊 |
| D、最外层电子数:甲>乙 |
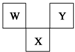 如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )
如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )| A、三种元素的原子半径的大小顺序是W<Y<X |
| B、X元素的氧化物、氢化物的水溶液都呈酸性 |
| C、Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质 |
| D、W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性 |
能正确表示下列反应的离子方程式是( )
| A、硫化氢气体通入硫酸铜溶液中:H2S+Cu2+=CuS↓+2H+ |
| B、铁与足量稀硝酸反应:Fe+4H++NO3-=Fe2++4H2O+NO↑ |
| C、醋酸溶解大理石:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、等物质的量的Ba(OH)2与Al2(SO4)3在溶液中反应:Ba2++3OH-+Al3++SO42-=BaSO4↓+Al(OH)3↓ |
不能通过一次反应直接实现变化的是( )
①N2→NO2 ②S→SO2 ③NH3→NO ④NO→HNO3 ⑤HNO3→NO.
①N2→NO2 ②S→SO2 ③NH3→NO ④NO→HNO3 ⑤HNO3→NO.
| A、①⑤ | B、②⑤ | C、①④ | D、③④ |