题目内容
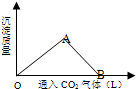
如图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线.试回答:
OA段曲线和AB段曲线所表示的反应方程式是:
OA段______;AB段______;OA段=AB段原因是______
B处溶液中存在的浓度较大的两种离子是______和______(填离子符号)
将B处生成的溶液煮沸,可见到的现象是______.
OA段曲线和AB段曲线所表示的反应方程式是:
OA段______;AB段______;OA段=AB段原因是______
B处溶液中存在的浓度较大的两种离子是______和______(填离子符号)
将B处生成的溶液煮沸,可见到的现象是______.

OA段:在Ca(OH)2溶液中通入二氧化碳气体,先生成CaCO3(不溶于水),反应的离子方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
AB段:当碱消耗完,再通入二氧化碳,二氧化碳与碳酸钙、水继续反应生成Ca(HCO3)2(溶于水),反应离子方程式为:Ca(HCO3)2=CaCO3↓+CO2↑+H2O;
根据反应的离子方程式可知,生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等,所以OA段=AB段;
B处氢氧化钙与二氧化碳恰好完全反应生成了碳酸氢钙,浓度较大的两种离子为:Ca2+;HCO3-;
将B处生成的溶液煮沸,由于碳酸氢钙不稳定,加热时易分解,又转化为碳酸钙,
故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;Ca(HCO3)2=CaCO3↓+CO2↑+H2O;生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等;
Ca2+;HCO3-;有白色沉淀生成.
AB段:当碱消耗完,再通入二氧化碳,二氧化碳与碳酸钙、水继续反应生成Ca(HCO3)2(溶于水),反应离子方程式为:Ca(HCO3)2=CaCO3↓+CO2↑+H2O;
根据反应的离子方程式可知,生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等,所以OA段=AB段;
B处氢氧化钙与二氧化碳恰好完全反应生成了碳酸氢钙,浓度较大的两种离子为:Ca2+;HCO3-;
将B处生成的溶液煮沸,由于碳酸氢钙不稳定,加热时易分解,又转化为碳酸钙,
故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;Ca(HCO3)2=CaCO3↓+CO2↑+H2O;生成CaCO3沉淀和CaCO3沉淀溶解所消耗的二氧化碳的量相等;
Ca2+;HCO3-;有白色沉淀生成.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目