题目内容
常温下,下列各组粒子在指定溶液中能大量共存的是
- A.pH=l的溶液中:CH3CH2OH、Cr2O72-、K+、SO42-
- B.NaHCO3溶液中:
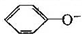 、CO32-、Br-、K+
、CO32-、Br-、K+ - C.加入铝粉放出大量H2的溶液中:Fe2+、K+、Cl-、NO3-
- D.C(Ca2+)=0.1 mol?L-1的溶液中:NH4+、SiO32-、CH3COO-、Br-
B
分析:A.pH=l的溶液,显酸性,利用氧化还原反应来分析;
B.该组离子之间不反应;
C.加入铝粉放出大量H2的溶液,为酸或强碱溶液;
D.硅酸钙不溶于水.
解答:A.pH=l的溶液,显酸性,CH3CH2OH、Cr2O72-发生氧化还原反应,则一定不能共存,故A错误;
B.该组离子之间不反应,则能够大量共存,故B正确;
C.加入铝粉放出大量H2的溶液,为酸或强碱溶液,酸溶液中Fe2+、NO3-发生氧化还原反应不生成氢气,Al、NO3-发生氧化还原反应不生成氢气,碱溶液中OH-与Fe2+结合生成沉淀,则一定不能大量共存,故C错误;
D.C(Ca2+)=0.1 mol?L-1的溶液置换,Ca2+、SiO32-结合硅酸钙沉淀,则一定不能共存,故D错误;
故选B.
点评:本题考查离子的共存问题,明确信息来判断溶液的酸碱性是解答本题的关键,熟悉离子之间的反应即可解答,题目难度不大.
分析:A.pH=l的溶液,显酸性,利用氧化还原反应来分析;
B.该组离子之间不反应;
C.加入铝粉放出大量H2的溶液,为酸或强碱溶液;
D.硅酸钙不溶于水.
解答:A.pH=l的溶液,显酸性,CH3CH2OH、Cr2O72-发生氧化还原反应,则一定不能共存,故A错误;
B.该组离子之间不反应,则能够大量共存,故B正确;
C.加入铝粉放出大量H2的溶液,为酸或强碱溶液,酸溶液中Fe2+、NO3-发生氧化还原反应不生成氢气,Al、NO3-发生氧化还原反应不生成氢气,碱溶液中OH-与Fe2+结合生成沉淀,则一定不能大量共存,故C错误;
D.C(Ca2+)=0.1 mol?L-1的溶液置换,Ca2+、SiO32-结合硅酸钙沉淀,则一定不能共存,故D错误;
故选B.
点评:本题考查离子的共存问题,明确信息来判断溶液的酸碱性是解答本题的关键,熟悉离子之间的反应即可解答,题目难度不大.

练习册系列答案
相关题目
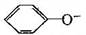 、CO32-、Br-、K+
、CO32-、Br-、K+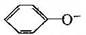 、CO32-、Br-、K+
、CO32-、Br-、K+