题目内容
某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
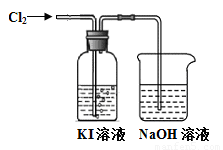
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)已知I2+I- I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3- , I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
| 操作 | 实验现象 |
a | 取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色, 水层显浅黄色。 |
b | 取2~3 mL饱和碘水,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色,水层几近无色。 |
① 实验b的目的是?? ?????????????????????????????????? ???? 。
② 根据实验a中,水层中含有的粒子有????????????????????????? 。
③ 实验a中水溶液颜色变浅的原因是????????????????????????????????? 。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为??????? 。
(2)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化。已知1 mol Cl2可氧化0.2 mol I2,该反应的化学方程式是????????????????????????????????? 。
(3) 根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为??????????????? 。
(1)① 对比实验,证明实验a中水层显浅黄色是因为存在I2+I- I3-平衡,不是单一的I2浓度降低所导致的。(2分)
I3-平衡,不是单一的I2浓度降低所导致的。(2分)
② I2、I-、I3-、Cl-、K+(可不写H2O、H+、OH-)(2分)
③ 由于萃取使水溶液中I2浓度降低,同时I2+I- I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。(2分)
④ 取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(2分)
【或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。】
(2)I2+5Cl2+6H2O  10H Cl +2 H IO3(2分)
10H Cl +2 H IO3(2分)
(3)溶液先变蓝后褪色(1分)
【解析】
试题分析:(1)①? 实验b的目的是对比实验,证明实验a中水层显浅黄色是因为存在I2+I- I3-平衡,不是单一的I2浓度降低所导致的。
I3-平衡,不是单一的I2浓度降低所导致的。
② 根据实验a中,取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。因为KI+Cl2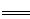 2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I-
2KCl+I2,水层中,含有含有Cl-、K+,水层显浅黄色,说明存在I2+I- I3-,对可逆反应I2、I-、I3-均存在;
I3-,对可逆反应I2、I-、I3-均存在;
③ 实验a中水溶液颜色变浅的原因是由于萃取使水溶液中I2浓度降低,同时I2+I- I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
I3-平衡逆向向移动,I3-浓度也降低,导致水溶液颜色变浅。
④ 为保证实验的严谨性,在实验a、b的基础上,需补充检验I-或I2的实验,所以答案是取2~3 mL KI溶液,滴加少量的氯水(或通入少量氯气,或加入少量碘单质),再加入足量CCl4, 振荡静置,观察到水层是否为黄色。(或取少量实验a的水层溶液滴加AgNO3溶液,观察是否有黄色沉淀生成。或取少量实验a的水层溶液淀粉溶液,观察是否变蓝。)
(2)已知1 mol Cl2可氧化.2 mol I2,知Cl2和I2的系数比是5:1,根据氧化还原反应特点,化合价升降总数相等,判断出I2变为+5价,配平得I2+5Cl2+6H2O  10HCl +2H IO3;
10HCl +2H IO3;
(3)向淀粉-KI溶液中持续通入氯气,可能观察到的现象为溶液先变蓝,I2+5Cl2+6H2O  10HCl +2HIO3所以后褪色;
10HCl +2HIO3所以后褪色;
考点:考查探究实验和实验方案的设计。

