题目内容
【题目】下列说法正确的是
A.pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-6molL-1
B.浓度均为0.1 molL-1的CuSO4和(NH4)2SO4的混合溶液中:c(NH4+)>c(SO42-)>c(Cu2+)>c(H+)
C.0.1 molL-1NaF溶液中加入NH4Cl至中性:c(HF)=c(NH3H2O)
D.0.100 molL-1的Na2S溶液中通入HCl气体,至c(Cl-)=0.100 molL-1(忽略溶液体积的变化及H2S的挥发):c(OH-)-c(H+)=c(HS-)-c(S2-)
【答案】C
【解析】
A. pH=6的NaHSO3溶液中氢离子的浓度为10-6molL-1 ,氢氧根离子的浓度为10-8molL-1 ,根据电荷守恒得:c(H+)+c(Na+)=2c(SO32-)+c(HSO3-)+c(OH-),根据物料守恒得:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),两式联立得:c(SO32-)-c(H2SO3)=c(H+)-c(OH-)=10-6molL-1-10-8molL-1=9.9×10-7molL-1,A项错误;
B. NH4+和Cu2+水解,使溶液均显酸性,但水解程度不大,硫酸根离子不会水解,浓度均为![]() 的CuSO4和(NH4)2SO4的混合溶液中:c(SO42-) > c(NH4+) >c(Cu2+)>c(H+),B项错误;
的CuSO4和(NH4)2SO4的混合溶液中:c(SO42-) > c(NH4+) >c(Cu2+)>c(H+),B项错误;
C.根据电荷守恒有:c(H+)+c(NH4+)+c(Na+)=c(F-)+c(Cl-)+c(OH-),溶液显中性,c(H+)= c(OH-),所以c(NH4+)+c(Na+)=c(F-)+c(Cl-),根据物料守恒有:c(Cl-)=c(NH3H2O)+c(NH4+),c(Na+)=c(F-)+c(HF),因此有c(HF)=c(NH3H2O),C项正确;
D. c(Cl-)=0.100 molL-1的溶液中,c(S2-)+c(HS-)+c(H2S)=c(Cl-)=0.100 molL-1,又因c(Cl-)+c(OH-)=c(H+)+c(HS-)+2c(H2S),所以c(OH-)-c(H+)=c(HS-)+2c(H2S)-[ c(S2-)+c(HS-)+c(H2S)]=c(H2S)-c(S2-),D项错误;
答案选C。

【题目】为了缓解温空效应,科学家提出了多种回收和利用![]() 的方案。
的方案。
![]() 方案1:利用FeO吸收
方案1:利用FeO吸收![]() 获得
获得![]()
![]()
![]()
则![]() ______。
______。
方案2:利用![]() 制备
制备![]()
![]() 时,向2L恒容密闭容器中充入
时,向2L恒容密闭容器中充入![]() 和
和![]() 发生反应:
发生反应:![]() ,混合气体中
,混合气体中![]() 的浓度与反应时间的关系如图1所示。
的浓度与反应时间的关系如图1所示。
![]() ①从反应开始到恰好达到平衡时,
①从反应开始到恰好达到平衡时,![]() 的平均反应速率
的平均反应速率![]() ______。
______。
②![]() 时,反应的平衡常数
时,反应的平衡常数![]() ______。
______。
③保持温度不变,向平衡后的容器中再充入![]() 和
和![]() ,重新达到平衡时
,重新达到平衡时![]() 的浓度______
的浓度______![]() 填序号
填序号![]() 。
。
A.等于![]()
![]() 等于
等于![]()
![]()
![]() 大于
大于![]()
![]() 时,如果该容器中有
时,如果该容器中有![]() 、
、![]() 、
、![]() 、
、![]() 。则
。则![]() ______
______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() “
“![]() 。
。
![]() 已知:
已知:![]() 时,该反应的平衡常数
时,该反应的平衡常数![]() 则
则![]() ______
______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
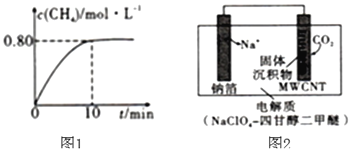
方案3:利用“![]() ”电池将
”电池将![]() 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“![]() ”电池以钠箔和多壁碳纳米管
”电池以钠箔和多壁碳纳米管![]() 为电极材料,总反应为
为电极材料,总反应为![]()
![]()
![]() 放电时该电池“吸入”
放电时该电池“吸入”![]() ,其工作原理如图2所示:
,其工作原理如图2所示:![]() 假设开始时两极的质量相等
假设开始时两极的质量相等![]()
![]() ①放电时,正极的电极反应式为______。
①放电时,正极的电极反应式为______。
②若生成的![]() 和C全部沉积在电极表面,当转移
和C全部沉积在电极表面,当转移![]() 时,两极的质量差为______g。
时,两极的质量差为______g。
![]() 室温下,物质的量浓度均为
室温下,物质的量浓度均为![]() 的几种含碳盐溶液的pH如下表:
的几种含碳盐溶液的pH如下表:
序号 | ① | ② | ③ |
溶液 |
| NaX |
|
pH |
|
|
|
写出溶液②中通入少量![]() 的离子方程式:______;等体积的①和③形成的混合溶液中离子浓度由大到小排列为:______
的离子方程式:______;等体积的①和③形成的混合溶液中离子浓度由大到小排列为:______