题目内容
恒温恒压下,在容积可变的密闭容器中发生反应:A(g)+B(g)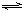 C(g)。若开始时通入1molA和1molB,达到平衡后生成amolC,则下列说法错误的是( )。
C(g)。若开始时通入1molA和1molB,达到平衡后生成amolC,则下列说法错误的是( )。A.若开始通入3molA和3molB,达到平衡后将生成3amolC
B.若开始通入xmolA、2molB和1molC,达到平衡后密闭容器中有1molA和3molC,则x为3
C.若开始时通入4molA、2molB和1molC,达到平衡时,B的物质的量一定大于2mol
D.若开始时通入2molA、2molB和1molC,达到平衡后,再通入3molC,则再次达到平衡后,C的物质的量分数为a/(2-a)
BC
【试题分析】
本题是一道综合题,A设计了等效平衡,恒温恒压时,当起始反应物或生成物的物质的量之比(不一定要求与化学计量数之比相同)相同时,即建立等效平衡。达到平衡时,混合物中各组分的百分含量相等,各物质的物质的量与起始量成正比;B是考查平衡移动的极值问题,当生成了3molC,就要消耗2molB,平衡时B为0,这不可能;C中达到平衡时,B的物质的量一定大于2mol,也就是反应要向逆反应方向移动,没有任何条件和理由证明平衡要逆向移动;D还是从等效平衡考虑,2molA、2molB和1molC换算到左边就是3molA和3molB,再通入3molC,等同于开始加入6molA、6molB,平衡时生成6amolC,这样A和B物质的量都是(6-6a)mol,可计算出C的物质的量分数为a/(2-a),故答案应是BC。

练习册系列答案
相关题目
 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。  4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。