题目内容
两种不同形态的氧化铝的部分性质如下表:
| 物质 | α-Al2O3 | γ-Al2O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α-Al2O3 |
| 温度/℃ 溶解度/g |
0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
②“焙烧”温度过高,会导致硫酸铝晶体产量降低,其原因是
(2)从“母液”制备硫酸铝晶体的实验步骤为:①
(3)测定硫酸铝晶体样品中Al2(SO4)3?18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25mL水中.
步骤2:加入c1 mol?L-1EDTA溶液V1mL(过量),煮沸、冷却,稀释至100mL.
步骤3:取25.00mL上述稀释液,滴加指示剂,用c2 mol?L-1 Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗v2mL Pb(NO3)2标准溶液.
①步骤2中“稀释至100mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
②根据上述数据计算,该样品中Al2(SO4)3?18H2O的质量分数为
③若样品中含有可与EDTA反应的杂质离子,所测定的Al2(SO4)3?18H2O的质量分数将会
②温度过高导致γ-A12O3转化为难溶于硫酸的α-Al2O3;
(2)根据从溶液中制取晶体的步骤来分析;
(3)①根据仪器的作用选取仪器;
②根据硝酸铅的物质的量计算参加反应的EDTA的物质的量,再根据剩余EDTA的物质的量计算参加反应的铝离子的物质的量,根据质量分数公式计算其质量分数;
③若样品中含有可与EDTA反应的杂质离子,导致EDTA的量增大,则测定的硫酸铝的物质的量偏高.
所以硫酸铝和明矾的物质的量之比为1:1,故答案为:1:1;
②“焙烧”温度过高,γ-A12O3转化为难溶于硫酸的α-Al2O3,会导致硫酸铝晶体产量降低,
故答案为:γ-A12O3转化为难溶于硫酸的α-Al2O3;
(2)从溶液中制取硫酸铝晶体时要经过蒸发浓缩溶液、冷却结晶、过滤、洗涤、干燥,故答案为:①蒸发浓缩;②冷却结晶;
(3)①配制一定物质的量浓度的溶液时,用100mL容量瓶配制溶液,用胶头滴管定容,故答案为:100 mL容量瓶、胶头滴管;
②硝酸铅和EDTA反应时需要EDTA的物质的量=10-3C2V2mol,那么100mL溶液中EDTA的物质的量=4×10-3C2V2mol,则和铝离子反应的EDTA的物质的量=10-3C1V1mol-4×10-3C2V2mol,EDTA和铝离子以1:1反应,所以铝离子的物质的量=10-3C1V1mol-4×10-3C2V2mol,Al2(SO4)3?18H2O的物质的量=0.5×(10-3C1V1mol-4×10-3C2V2mol),Al2(SO4)3?18H2O的质量=0.5×(10-3C1V1mol-4×10-3C2V2mol)×666g/mol=333(10-3C1V1-4×10-3C2V2)g,
其质量分数=
| 333(C1V1-4C2V2) |
| 103m |
故答案为:
| 333(C1V1-4C2V2) |
| 103m |
③若样品中含有可与EDTA反应的杂质离子,导致EDTA的使用量增大,从而导致铝离子的质量数偏高,故答案为:偏高.

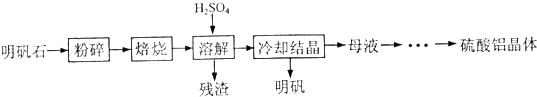
(14分)以明矾石[主要成分为K2SO4·Al2(SO4)3·2A12O3·6H2O]为原料生产硫酸铝晶体[Al2(SO4)3·18H2O]和明矾[KAl(SO4)2·12H2O]的实验流程如下: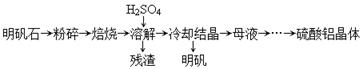
两种不同形态的氧化铝的部分性质如下表:
| 物质 | α-Al2O3 | γ-A12O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α- Al2O3 |
| 温度/℃ 溶解度/g | 0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
(2)从“母液”制备硫酸铝晶体的实验步骤为:① ;② ;③过滤、洗涤、干燥。
(3)测定硫酸铝晶体样品中Al2(SO4)3·18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25 mL水中。
步骤2:加入c1 mo1·L-1EDTA溶液V1mL(过量),煮沸、冷却,稀释至100 mL。
步骤3:取25. 00mL上述稀释液,滴加指示剂,用c2 mol·L-1Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗v2mL Pb(NO3)2标准溶液。
①步骤2中“稀释至100 mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、 。
②根据上述数据计算,该样品中Al2(SO4)3·18H2O的质量分数为 。(用含字母的代数式表示)。
(4)铝的阳极氧化法是把铝作为阳极,置于硫酸等电解液中,施加阳极电压进行电解,在铝的表面形成一层致密的氧化膜。
①电解过程中阳极的电极反应为 。
②取少量废电解液,加入NaHCO,溶液后产生气泡和白色沉淀,产生沉淀的原因是 。(用离子方程式表示)
(14分)以明矾石[主要成分为K2SO4·Al2(SO4)3·2A12O3·6H2O]为原料生产硫酸铝晶体[Al2(SO4)3·18H2O]和明矾[KAl(SO4)2·12H2O]的实验流程如下:
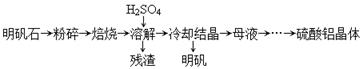
两种不同形态的氧化铝的部分性质如下表:
|
物质 |
α-Al2O3 |
γ-A12O3 |
|
性质 |
不溶于水和酸 |
不溶于水,溶于强酸或强碱,加热至1200℃可转化为α- Al2O3 |
Al2(SO4)3、明矾在不同温度下的溶解度如下表:
|
温度/℃ 溶解度/g |
0 |
20 |
40 |
60 |
80 |
100 |
|
Al2(SO4)3 |
31.2 |
36.4 |
46.1 |
59.2 |
73.0 |
89.0 |
|
明矾 |
3.0 |
5.9 |
11.7 |
25 |
71 |
154 |
(1) “焙烧’’温度过高,会导致硫酸铝晶体产量降低,其原因是 。
(2)从“母液”制备硫酸铝晶体的实验步骤为:① ;② ;③过滤、洗涤、干燥。
(3)测定硫酸铝晶体样品中Al2(SO4)3·18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25 mL水中。
步骤2:加入c1 mo1·L-1EDTA溶液V1mL(过量),煮沸、冷却,稀释至100 mL。
步骤3:取25. 00mL上述稀释液,滴加指示剂,用c2 mol·L-1Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗v2mL Pb(NO3)2标准溶液。
①步骤2中“稀释至100 mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、 。
②根据上述数据计算,该样品中Al2(SO4)3·18H2O的质量分数为 。(用含字母的代数式表示)。
(4)铝的阳极氧化法是把铝作为阳极,置于硫酸等电解液中,施加阳极电压进行电解,在铝的表面形成一层致密的氧化膜。
①电解过程中阳极的电极反应为 。
②取少量废电解液,加入NaHCO,溶液后产生气泡和白色沉淀,产生沉淀的原因是 。(用离子方程式表示)