题目内容
下列离子方程式书写正确的是
A.实验室用氯化铁溶液制取氢氧化铁胶体:Fe3++3H2O Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| B.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C.铝和烧碱溶液:2Al+2OH-+2H2O=2Al3++3H2↑ |
| D.AlCl3溶液中加入过量氨水:Al3++4OH- =AlO2-+2H2O |
A
解析试题分析:判断离子方程式正确与否的方法一般是:(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式。A、氢氧化铁胶体不能拆开,所以实验室用氯化铁溶液制取氢氧化铁胶体的离子方程式为Fe3++3H2O Fe(OH)3(胶体)+3H+,A正确;B、醋酸是弱酸不能拆开,则碳酸钙溶于醋酸的离子方程式为CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,B不正确;C、铝与烧碱反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,C不正确;D、氨水是弱碱不能溶解氢氧化铝,则AlCl3溶液中加入过量氨水的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+,D不正确,答案选A。
Fe(OH)3(胶体)+3H+,A正确;B、醋酸是弱酸不能拆开,则碳酸钙溶于醋酸的离子方程式为CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,B不正确;C、铝与烧碱反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,C不正确;D、氨水是弱碱不能溶解氢氧化铝,则AlCl3溶液中加入过量氨水的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+,D不正确,答案选A。
考点:考查离子方程式的正误判断

练习册系列答案
相关题目
下列各组中两种物质在溶液的反应,能用同一离子方程式表示的是
| A.铁和稀盐酸、铁和稀硝酸 |
| B.铜和浓硝酸、铜和稀硝酸 |
| C.NaHCO3+ NaOH;NaHSO4+ NaOH |
| D.BaCl2+ H2SO4; Ba(OH)2+ Na2SO4 |
在指定的条件下,下列各组离子一定能大量共存的是
| A.无色的溶液中:Fe3+、K+、NO3-、Cl- |
| B.pH=13的溶液中:NH4+、Na+、SO42-、Cl- |
| C.含有大量Ba2+ 的溶液中:NH4+、Na+、Cl-、H+ |
| D.c(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO3- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- |
| B.加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C.0.1 mol·L-1NaAlO2溶液:Al3+、Na+、Cl-、NO3- |
| D.水电离出的c(H+)=10-12 mol·L-1的溶液:Na+、K+、NH4+、CO32- |
在透明溶液中,下列各组离子能大量共存的是
| A.HCO3-、ClO-、K+、H+ | B.Na+、Fe2+、NO3-、H+ |
| C.K+、Cu2+、Cl-、SO42- | D.OH-、NH4+、Cl-、SO32- |
下列离子方程式中,书写正确的是
A.弱酸酸式盐NaHB在水溶液中水解:HB–+H2O H3O++B2– H3O++B2– |
B.电解饱和食盐水:C1-+2H2O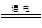 H2↑+Cl2↑+OH- H2↑+Cl2↑+OH- |
| C.氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- |
| D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
| A.Na+ | B.CO32-、NH4+ | C.CH3COO- | D.CH3COO-、Na+ |
解释下列现象的化学用语正确的是( )
A.铁钉在空气中出现红色的铁锈,其负极反应式为:Fe-3e- Fe3+ Fe3+ |
B.氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2N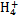  Mg2++2NH3·H2O Mg2++2NH3·H2O |
C.SO2通入到滴加酚酞的NaOH溶液中,红色变浅:SO2+2OH- S S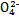 +H2O +H2O |
D.向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2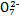 +H2O +H2O 2Cr 2Cr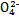 +2H+ +2H+ |
