题目内容
【题目】在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分。下列说法不正确的是( )
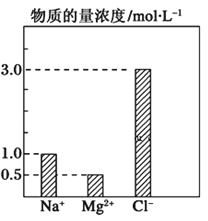
A. NaCl的物质的量为0.2mol
B. 溶质MgCl2的质量为9g
C. 该混合液中BaCl2的物质的量为0.1mol
D. 将该混合液加水稀释至体积为1L,稀释后溶液中Ba2+的物质的量浓度为0.1mol/L
【答案】B
【解析】A项,n(Na+)=1.0mol/L![]() 0.2L=0.2mol,NaCl物质的量为0.2mol,正确;B项,n(Mg2+)=0.5mol/L
0.2L=0.2mol,NaCl物质的量为0.2mol,正确;B项,n(Mg2+)=0.5mol/L![]() 0.2L=0.1mol,n(MgCl2)=0.1mol,m(MgCl2)=0.1mol
0.2L=0.1mol,n(MgCl2)=0.1mol,m(MgCl2)=0.1mol![]() 95g/mol=9.5g,错误;C项,根据电荷守恒,c(Na+)+2c(Mg2+)+2c(Ba2+)=c(Cl-),c(Ba2+)=(3.0mol/L-1.0mol/L-0.5mol/L
95g/mol=9.5g,错误;C项,根据电荷守恒,c(Na+)+2c(Mg2+)+2c(Ba2+)=c(Cl-),c(Ba2+)=(3.0mol/L-1.0mol/L-0.5mol/L![]() 2)
2)![]() 2=0.5mol/L,n(BaCl2)=n(Ba2+)=0.5mol/L
2=0.5mol/L,n(BaCl2)=n(Ba2+)=0.5mol/L![]() 0.2L=0.1mol,正确;D项,稀释前后溶质物质的量不变,则稀释后Ba2+物质的量浓度为0.1mol
0.2L=0.1mol,正确;D项,稀释前后溶质物质的量不变,则稀释后Ba2+物质的量浓度为0.1mol![]() 1L=0.1mol/L,正确;答案选B。
1L=0.1mol/L,正确;答案选B。

练习册系列答案
相关题目