题目内容
影响化学反应速率的因素有多方面,如浓度、压强、温度、催化剂等.下列有关说法不正确的是( )
分析:A、升高温度增大单位体积内的活化分子数目;
B、浓度增大,活化分子百分数不变,增大单位体积内分子总数,增大加了单位体积内活化分子的数目;
C、压强改变不能引起气体物质浓度的变化,不能影响气体的反应速率;
D、催化剂改变反应历程,降低反应的活化能.
B、浓度增大,活化分子百分数不变,增大单位体积内分子总数,增大加了单位体积内活化分子的数目;
C、压强改变不能引起气体物质浓度的变化,不能影响气体的反应速率;
D、催化剂改变反应历程,降低反应的活化能.
解答:解:A、升高温度,增大活化分子百分数,增大单位体积内的活化分子数目,有效碰撞增大,反应速率加快,故A错误;
B、浓度增大,活化分子百分数不变,增大单位体积内分子总数,增大加了单位体积内活化分子的数目,有效碰撞增大,反应速率加快,故B正确;
C、恒温恒容下,通入不反应的气体,增大压强,反应气体物质的浓度不变,气体的反应速率不变,故C错误;
D、催化剂改变反应历程,降低反应的活化能,增大活化分子百分数,增大单位体积内的活化分子数目,有效碰撞增大,反应速率加快,故D错误;
故选B.
B、浓度增大,活化分子百分数不变,增大单位体积内分子总数,增大加了单位体积内活化分子的数目,有效碰撞增大,反应速率加快,故B正确;
C、恒温恒容下,通入不反应的气体,增大压强,反应气体物质的浓度不变,气体的反应速率不变,故C错误;
D、催化剂改变反应历程,降低反应的活化能,增大活化分子百分数,增大单位体积内的活化分子数目,有效碰撞增大,反应速率加快,故D错误;
故选B.
点评:本题考查化学反应速率的影响因素,有效碰撞理论等,难度不大,注意利用有效碰撞理论理解外界条件对反应速率的影响.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
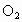 中比在空气中燃烧剧烈._______
中比在空气中燃烧剧烈._______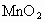 加入双氧水中反应更剧烈________
加入双氧水中反应更剧烈________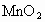 加入
加入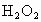 中反应更加剧烈__________.
中反应更加剧烈__________.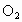 中比在空气中燃烧剧烈._______
中比在空气中燃烧剧烈._______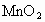 加入双氧水中反应更剧烈________
加入双氧水中反应更剧烈________