题目内容
【题目】芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。
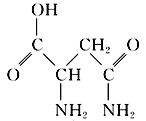
(1)天冬酰胺所含元素中,________(填元素名称,下同)元素基态原子核外未成对电子数最多,第一电离能最大的是________。
(2)天冬酰胺中碳原子的杂化轨道类型为________,分子中σ键和π键数目之比为________。
(3)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表。
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为________________________________________。
H2O、H2S、H2Se沸点由高到低的顺序为________________,酸性由强到弱的顺序为________________。
(4)写出铬的基态原子电子排布式:________________________________________。
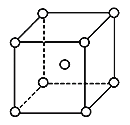
(5)铬为体心立方晶体,晶胞结构如图,则该晶胞中含有______个铬原子。若铬的密度为ρg·cm-3,相对原子质量为M,NA表示阿伏加德罗常数的值,则铬原子的半径为______cm。
【答案】 氮 氮 sp3和sp2 8∶1 由于硫的电负性强于Se,形成的共用电子对斥力大,键角大 H2O>H2Se>H2S H2Se>H2S>H2O 1s22s22p63s23p63d54s1或[Ar]3d54s1 2 ![]()
![]()
【解析】(1)天冬酰胺中含有H、C、N、O四种元素,原子基态核外未成对电子分别为1、2,3、2,因此氮元素基态原子核外未成对电子数最多。氮元素的2p轨道电子处于半充满状态,稳定性强,因此H、C、N、O第一电离能最大的是N;(2)分子中亚甲基和次甲基中的碳原子均为sp3杂化,羰基碳为sp2杂化,天冬酰胺中含有16个σ键和2个π键,因此σ和π键数目之比为8∶1;(3)硫原子的电负性强于Se,形成的共用电子对斥力大,因此H2S中键角大,H2O、H2S、H2Se均为分子晶体,由于水分子间存在氢键,因此其沸点高于H2S和H2Se,H2Se相对分子质量大于H2S,故沸点H2Se高于H2S,酸性由强到弱的顺序为H2Se>H2S>H2O;(4)铬的原子序数为24,根据构造原理其基态电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1;(5)在铬的晶胞中含有铬原子数为1+8×1/8=2,设晶胞边长为x,根据ρ=m/V
得,ρ=![]() ,所以x=
,所以x=![]() ,因此晶胞的休对角线长度为
,因此晶胞的休对角线长度为![]() ,所以钠原子半径=
,所以钠原子半径=![]() 。
。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案