题目内容
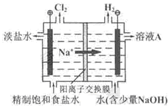 (2011?北京)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
(2011?北京)氯碱工业中电解饱和食盐水的原理示意图如右图所示.(1)溶液A的溶质是
NaOH
NaOH
.(2)电解饱和食盐水的离子方程式是
2Cl-+2H2O
H2↑+Cl2↑+2OH-
| ||
2Cl-+2H2O
H2↑+Cl2↑+2OH-
.
| ||
(3)电解时用盐酸控制阳极区溶液的pH在2~3.用化学平衡移动原理解释盐酸的作用:
Cl2与水的反应为Cl2+H2O HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
 HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出Cl2与水的反应为Cl2+H2O HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
. HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出(4)电解所用的盐水需精制,去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42-)>c(Ca2+)].精制流程如下(淡盐水和溶液A来自电解池):
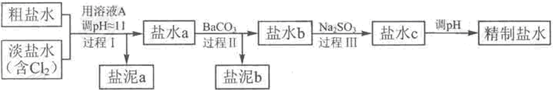
①盐泥a除泥沙外,还含有的物质是
Mg(OH)2
Mg(OH)2
.②过程I中将NH4+转化为N2的离子方程式是
2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O
2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O
.③BaSO4的溶解度比BaCO3的小.过程II中除去的离子有
SO42-、Ca2+
SO42-、Ca2+
.④经过程III处理,要求盐水c中剩余Na2SO3的含量小于5mg/L.若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b,至多添加10% Na2SO3溶液
1.76
1.76
kg(溶液体积变化忽略不计).分析:(1)根据电极反应判断阴极产物;
(2)根据两极的反应书写电解反应式;
(3)根据阳极产物和平衡移动原理分析;
(4)①根据杂质离子和溶液的酸碱性判断能反应生成的沉淀;
②根据A溶液成分和可能具有的性质,结合氧化还原反应和质量守恒定律书写离子方程式;
③根据溶液成分和溶解度大小判断生成的沉淀;
④根据反应方程式和质量守恒解答.
(2)根据两极的反应书写电解反应式;
(3)根据阳极产物和平衡移动原理分析;
(4)①根据杂质离子和溶液的酸碱性判断能反应生成的沉淀;
②根据A溶液成分和可能具有的性质,结合氧化还原反应和质量守恒定律书写离子方程式;
③根据溶液成分和溶解度大小判断生成的沉淀;
④根据反应方程式和质量守恒解答.
解答:解:(1)电解饱和食盐水时,阴极反应式为:2H2O-2e-═2OH-+H2↑,阳极反应式为:2Cl--2e-═Cl2↑,阴极产物为NaOH和H2,阳极产物是Cl2,据此可以确定溶液A的溶质是NaOH,故答案为:NaOH;
(2)根据阳极极和阴极的反应式可得电解反应的离子方程式是2Cl-+2H2O
H2↑+Cl2↑+2OH-,故答案为:2Cl-+2H2O
H2↑+Cl2↑+2OH-;
(3)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl2+H2O HCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,故答案为:Cl2与水的反应为Cl2+H2O
HCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,故答案为:Cl2与水的反应为Cl2+H2O HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出;
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出;
(4)①根据粗盐水和淡盐水的化学成分,代入题给精制盐水的流程进行分析,可知过程I是将Mg2+转化为Mg(OH)2沉淀除去,即盐泥a中除泥沙外,还含有的物质是Mg(OH)2,
故答案为:Mg(OH)2;
②将NH4+转化为N2的氧化剂是Cl2,对应的离子方程式是2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O,故答案为:2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O;
③过程II是利用沉淀溶解平衡原理,将溶液中的Ca2+和SO42-分别转化为CaCO3和BaSO4沉淀除去,故答案为:SO42-、Ca2+;
④NaClO与Na2SO3溶液反应的化学方程式为:NaClO+Na2SO3 NaCl+Na2SO4,若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b时至少需要10%Na2SO3溶液
NaCl+Na2SO4,若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b时至少需要10%Na2SO3溶液
×126g?mol-1×
=1.26kg,若盐水c中剩余Na2SO3的含量为5mg/L,则还需添加10% Na2SO3溶液50g÷10%=0.5kg,因此至多添加10%Na2SO3溶液
的质量为1.26kg+0.5kg=1.76kg.故答案为:1.76.
(2)根据阳极极和阴极的反应式可得电解反应的离子方程式是2Cl-+2H2O
| ||
| ||
(3)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl2+H2O
 HCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,故答案为:Cl2与水的反应为Cl2+H2O
HCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,故答案为:Cl2与水的反应为Cl2+H2O HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出;
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出;(4)①根据粗盐水和淡盐水的化学成分,代入题给精制盐水的流程进行分析,可知过程I是将Mg2+转化为Mg(OH)2沉淀除去,即盐泥a中除泥沙外,还含有的物质是Mg(OH)2,
故答案为:Mg(OH)2;
②将NH4+转化为N2的氧化剂是Cl2,对应的离子方程式是2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O,故答案为:2NH4++3Cl2+8OH-═N2↑+6Cl-+8H2O;
③过程II是利用沉淀溶解平衡原理,将溶液中的Ca2+和SO42-分别转化为CaCO3和BaSO4沉淀除去,故答案为:SO42-、Ca2+;
④NaClO与Na2SO3溶液反应的化学方程式为:NaClO+Na2SO3
 NaCl+Na2SO4,若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b时至少需要10%Na2SO3溶液
NaCl+Na2SO4,若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b时至少需要10%Na2SO3溶液| 74.5g |
| 74.5g?mol-1 |
| 100 |
| 10 |
的质量为1.26kg+0.5kg=1.76kg.故答案为:1.76.
点评:本题考查饱和食盐水的电解和粗盐的提纯,题目较为综合,注意平衡移动原理的应用以及物质的量应用于化学方程式的计算.做题时注意题中所给信息,用守恒的方法解答.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目