题目内容
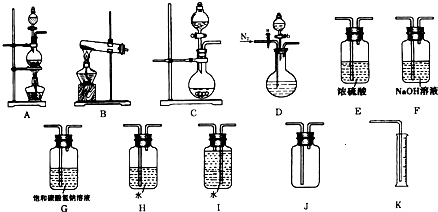
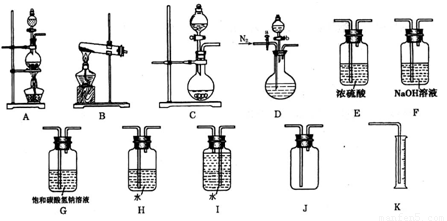
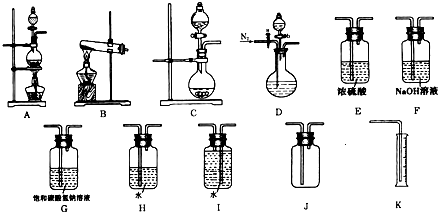
现有以下实验装置供实验时挑选使用.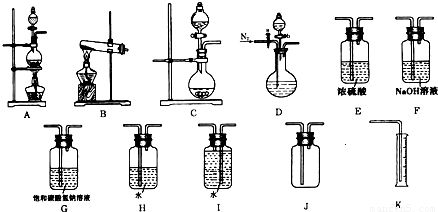
(1)利用Cu和浓硝酸反应制备NO2,用过氧化氢溶液和MnO2制取O2,根据反应原理应选用______装置(填序号,从A、B、C中选取).
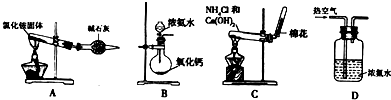
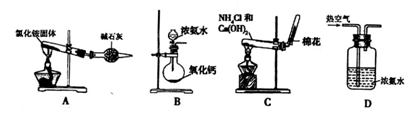
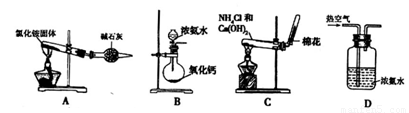
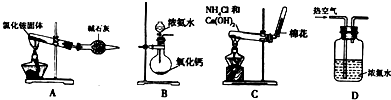
(2)某同学设计下列四种制备NH3的方法,不合理的是______(填序号)
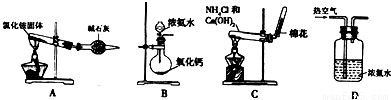
(3)欲用石灰石和浓盐酸反应制取纯净干燥的CO2气体,将你所选的仪器按气体由左向右方向连接,连接顺序为______.
用饱和碳酸氢钠溶液除去挥发出的HCl优于用水除HCl的原因是______.
(4)某小组为了探究Ag与浓硝酸反应过程中可能产生NO,设计了一连接顺序为D→H→I→K的实验装置.
①检验这一装置气密性的方法是______,
②反应开始前通入N2的目的是______,
③反应结束,若H瓶中溶液体积为100mL,从中取出25.00mL溶液以酚酞作指示剂,用0.1000mol?L-1NaOH溶液进行滴定,两次滴定用去NaOH溶液的体积分别为16.98%mL和17.0.2mL,则该瓶中硝酸的物质的量浓度为______.若实验测得NO的体积为95.2mL(已折算成标准状况),请你通过数据说明Ag与浓硝酸反应过程中是否有NO产生______.
【答案】分析:(1)根据反应物的状态和反应条件选取反应装置;
(2)根据反应物的特点分析;
(3)欲用石灰石和浓盐酸反应制取纯净干燥的CO2气体,根据反应物的状态和反应条件选取反应装置,要用碳酸氢钠溶液除去氯化氢,用浓硫酸干燥二氧化碳,根据二氧化碳的密度确定收集方法;
(4)①装置气密性检查的原理一般是通过压强差来产生明显的现象来判断;
②一氧化氮易被氧气氧化;
③根据硝酸和氢氧化钠的关系式计算硝酸的物质的量浓度,根据氮原子守恒确定是否有一氧化氮生成.
解答:解:(1)用Cu和浓硝酸反应制备NO2,用过氧化氢溶液和MnO2制取O2,都是固体混合不需加热,故选C;
(2)A.加热时,氯化铵分解生成氨气和氯化氢,当混合气体达到试管口时,温度降低,氯化氢和氨气反应生成氯化铵,所以得不到氨气,故错误;
B.氧化钙和水反应生成氢氧化钙且放出热量,放出的热量促使一水合氨分解生成氨气,所以能得到氨气,故正确;
C.氯化铵和氢氧化钙反应生成氯化钙和氨气,所以能得到氨气,故正确;
D.热空气能促进一水合氨分解生成氨气,但氨气中含有氧气、氮气等杂质,故错误;
故选AD.
(3)石灰石和浓盐酸制取二氧化碳是固液混合且不需加热的反应,所以反应装置选取C,浓盐酸、水具有挥发性,石灰石和浓盐酸反应是放热反应,所以生成的二氧化碳中含有氯化氢、水蒸气,为了制取纯净、干燥的二氧化碳,应该用饱和的碳酸氢钠溶液除去氯化氢,浓硫酸和二氧化碳不反应,所以用浓硫酸干燥二氧化碳,二氧化碳和空气不反应,且密度大于空气,所以可以采用向上排空气法收集,故选J,所以其连接顺序是C-G-E-J,
二氧化碳能和水反应,氯化氢和碳酸氢钠反应能生成二氧化碳,不仅除去氯化氢还能增加二氧化碳的量,所以用碳酸氢钠溶液除去氯化氢,
故答案为:C-G-E-J,不消耗二氧化碳,氯化氢能与碳酸氢钠反应生成二氧化碳;
(4)①装置气密性检查的原理一般是通过压强差来产生明显的现象来判断,检验方法为:关闭活塞a、b,微热烧瓶D,H装置长导管有气泡产生,I装置长导管一段时间液面高于集气瓶内液面,说明气密性良好,
故答案为:关闭活塞a、b,微热烧瓶D,H装置长导管有气泡产生,I装置长导管一段时间液面高于集气瓶内液面,说明气密性良好;
②空气中含有氧气,能氧化一氧化氮生成二氧化氮,为防止一氧化氮被氧化,充入氮气排出装置内残留的空气,
故答案为:排尽装置内残留的空气;
③使用氢氧化钠的平均体积=(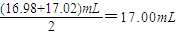 ,根据氢氧化钠和硝酸的关系式得硝酸的物质的量浓度=
,根据氢氧化钠和硝酸的关系式得硝酸的物质的量浓度=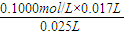 =0.068mol/L,实验测得的一氧化氮的物质的量=
=0.068mol/L,实验测得的一氧化氮的物质的量=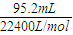 =0.00425mol,
=0.00425mol,
3NO2+H2O=2HNO3+NO,二氧化氮产生的一氧化氮的物质的量=0.5n(HNO3)=0.5×0.1L×0.0680mol/L=0.0034mol<0.00425,所以有一氧化氮生成,
故答案为:0.068mol/L;有.
点评:本题考查了气体的制取、干燥和收集装置的选取,根据反应物和生成物的状态、反应条件选取反应装置即可,根据气体的性质来选取收集装置,难点是物质的量的有关计算,根据原子守恒来分析解答,难度中等.
(2)根据反应物的特点分析;
(3)欲用石灰石和浓盐酸反应制取纯净干燥的CO2气体,根据反应物的状态和反应条件选取反应装置,要用碳酸氢钠溶液除去氯化氢,用浓硫酸干燥二氧化碳,根据二氧化碳的密度确定收集方法;
(4)①装置气密性检查的原理一般是通过压强差来产生明显的现象来判断;
②一氧化氮易被氧气氧化;
③根据硝酸和氢氧化钠的关系式计算硝酸的物质的量浓度,根据氮原子守恒确定是否有一氧化氮生成.
解答:解:(1)用Cu和浓硝酸反应制备NO2,用过氧化氢溶液和MnO2制取O2,都是固体混合不需加热,故选C;
(2)A.加热时,氯化铵分解生成氨气和氯化氢,当混合气体达到试管口时,温度降低,氯化氢和氨气反应生成氯化铵,所以得不到氨气,故错误;
B.氧化钙和水反应生成氢氧化钙且放出热量,放出的热量促使一水合氨分解生成氨气,所以能得到氨气,故正确;
C.氯化铵和氢氧化钙反应生成氯化钙和氨气,所以能得到氨气,故正确;
D.热空气能促进一水合氨分解生成氨气,但氨气中含有氧气、氮气等杂质,故错误;
故选AD.
(3)石灰石和浓盐酸制取二氧化碳是固液混合且不需加热的反应,所以反应装置选取C,浓盐酸、水具有挥发性,石灰石和浓盐酸反应是放热反应,所以生成的二氧化碳中含有氯化氢、水蒸气,为了制取纯净、干燥的二氧化碳,应该用饱和的碳酸氢钠溶液除去氯化氢,浓硫酸和二氧化碳不反应,所以用浓硫酸干燥二氧化碳,二氧化碳和空气不反应,且密度大于空气,所以可以采用向上排空气法收集,故选J,所以其连接顺序是C-G-E-J,
二氧化碳能和水反应,氯化氢和碳酸氢钠反应能生成二氧化碳,不仅除去氯化氢还能增加二氧化碳的量,所以用碳酸氢钠溶液除去氯化氢,
故答案为:C-G-E-J,不消耗二氧化碳,氯化氢能与碳酸氢钠反应生成二氧化碳;
(4)①装置气密性检查的原理一般是通过压强差来产生明显的现象来判断,检验方法为:关闭活塞a、b,微热烧瓶D,H装置长导管有气泡产生,I装置长导管一段时间液面高于集气瓶内液面,说明气密性良好,
故答案为:关闭活塞a、b,微热烧瓶D,H装置长导管有气泡产生,I装置长导管一段时间液面高于集气瓶内液面,说明气密性良好;
②空气中含有氧气,能氧化一氧化氮生成二氧化氮,为防止一氧化氮被氧化,充入氮气排出装置内残留的空气,
故答案为:排尽装置内残留的空气;
③使用氢氧化钠的平均体积=(
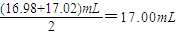 ,根据氢氧化钠和硝酸的关系式得硝酸的物质的量浓度=
,根据氢氧化钠和硝酸的关系式得硝酸的物质的量浓度=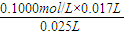 =0.068mol/L,实验测得的一氧化氮的物质的量=
=0.068mol/L,实验测得的一氧化氮的物质的量=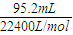 =0.00425mol,
=0.00425mol,3NO2+H2O=2HNO3+NO,二氧化氮产生的一氧化氮的物质的量=0.5n(HNO3)=0.5×0.1L×0.0680mol/L=0.0034mol<0.00425,所以有一氧化氮生成,
故答案为:0.068mol/L;有.
点评:本题考查了气体的制取、干燥和收集装置的选取,根据反应物和生成物的状态、反应条件选取反应装置即可,根据气体的性质来选取收集装置,难点是物质的量的有关计算,根据原子守恒来分析解答,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目