题目内容
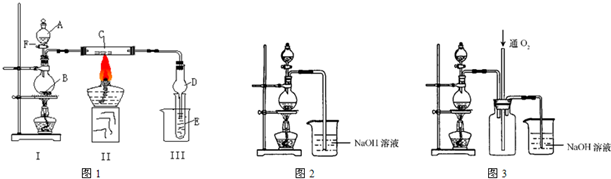
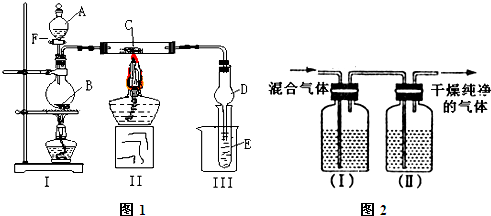
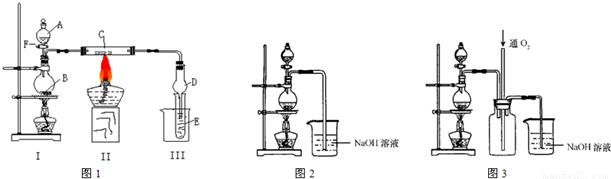
(I)按照如图1所示装置进行有关实验,拔掉分液漏斗玻璃塞,将A逐滴加入B中.
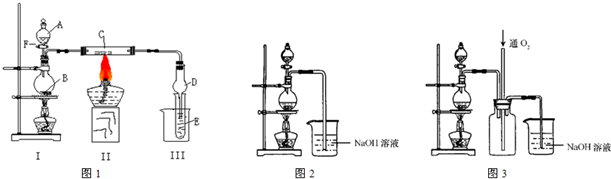
若A是浓盐酸,B为二氧化锰,当将A滴入B中时发生反应的离子方程式为:______;
当实验一段时间后,发现C、D中有红棕色烟,则C的化学式为:______.
(II)硫酸铜是一种应用极其广泛的化工原料,可通过多种途径制取硫酸铜晶体.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图2所示).
请回答相关问题:
(1)图2分液漏斗中装的液体是______;
(2)本实验中若硝酸过量,造成的结果是______;
(3)图3是图2的改进装置,其优点是①______,②______;
(4)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:将铜粉在某仪器中反复灼烧,使铜粉与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向混合物中加入Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,得硫酸铜晶体,滤渣循环使用〔已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4〕.
①方案1中用于灼烧铜粉的仪器名称是______;
②方案2中甲物质可以是______(填字母序号);
a.CuO b.CuCO3 c.CaCO3 d.NaOH
③方案2中发生反应的总化学方程式为(注明反应条件)______.
解:(I)二氧化锰与浓盐酸反应生成氯化锰、氯气、水,反应离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O.
Mn2++Cl2↑+2H2O.
实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,氯气与物质C反应生成FeCl3,故物质C为Fe.
故答案为:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;Fe.
Mn2++Cl2↑+2H2O;Fe.
(II)(1)由题目信息,实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,故图2分液漏斗中装的液体为浓硝酸.
故答案为:浓硝酸.
(2)硝酸过量制得的硫酸铜晶体中含有硝酸铜,制得的硫酸铜晶体不纯.
故答案为:制得的硫酸铜晶体不纯.
(3)反应中产生的尾气主要为NO,由于NO与NaOH溶液不反应,故应向氢氧化钠溶液中通入空气(氧气),装置3中在尾气吸收装置之前连接集气瓶,通入氧气有利于氮氧化合物的吸收,同时起安全瓶作用,防止倒吸.
故答案为:有利于氮氧化合物的吸收;防止倒吸.
(4)①高温灼烧固体应在坩埚中进行,方案1将铜粉在坩埚中反复灼烧,因此仪器应为坩埚.
故答案为:坩埚.
②由于溶液酸性较强,欲使Fe3+沉淀,需加入某种试剂降低c(H+)浓度,但又不能引入新杂质.
a.CuO降低c(H+)浓度,不引入新杂质,过量的CuO可以过滤除去,故a正确;
b.CuCO3 降低c(H+)浓度,不引入新杂质,过量的CuCO3 可以过滤除去,故b正确;
c.CaCO3 引入钙离子,故c错误;
d.NaOH引入钠离子,故d错误.
故选:ab.
③由题目信息可知,氧气直接通入到铜粉与稀硫酸的混合物,发生反应生成硫酸铜与水,
反应方程式为2Cu+O2+2H2SO4 2CuSO4+2H2O.
2CuSO4+2H2O.
故答案为:2Cu+O2+2H2SO4 2CuSO4+2H2O.
2CuSO4+2H2O.
分析:(I)二氧化锰与浓盐酸反应生成氯化锰、氯气、水.实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,即氯气与物质C反应生成FeCl3,据此物质C.
(II)(1)由题目信息,实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,判断图2分液漏斗中装的液体.
(2)硝酸过量制得的硫酸铜晶体中含有硝酸铜.
(3)装置3中在尾气吸收装置之前连接集气瓶,通入氧气有利于氮氧化合物的吸收,同时起安全瓶作用.
(4)①高温灼烧固体应在坩埚中进行.
②加入甲物质,目的是调节PH值,使Fe3+转化Fe(OH)3沉淀,且不能引入新杂质.
③由题目信息可知,氧气直接通入到铜粉与稀硫酸的混合物,发生反应生成硫酸铜与水.
点评:考查学生对实验原理的理解、实验方案的评价、实验装置的理解与评价、常用化学用语、物质推断、实验条件控制等,难度中等,实验方案设计,应根据实验目的思考实验原理,根据实验原理中反应物的状态和反应条件确定试剂和装置,通过比较和评价优选最佳实验方案.
 Mn2++Cl2↑+2H2O.
Mn2++Cl2↑+2H2O.实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,氯气与物质C反应生成FeCl3,故物质C为Fe.
故答案为:MnO2+4H++2Cl-
 Mn2++Cl2↑+2H2O;Fe.
Mn2++Cl2↑+2H2O;Fe.(II)(1)由题目信息,实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,故图2分液漏斗中装的液体为浓硝酸.
故答案为:浓硝酸.
(2)硝酸过量制得的硫酸铜晶体中含有硝酸铜,制得的硫酸铜晶体不纯.
故答案为:制得的硫酸铜晶体不纯.
(3)反应中产生的尾气主要为NO,由于NO与NaOH溶液不反应,故应向氢氧化钠溶液中通入空气(氧气),装置3中在尾气吸收装置之前连接集气瓶,通入氧气有利于氮氧化合物的吸收,同时起安全瓶作用,防止倒吸.
故答案为:有利于氮氧化合物的吸收;防止倒吸.
(4)①高温灼烧固体应在坩埚中进行,方案1将铜粉在坩埚中反复灼烧,因此仪器应为坩埚.
故答案为:坩埚.
②由于溶液酸性较强,欲使Fe3+沉淀,需加入某种试剂降低c(H+)浓度,但又不能引入新杂质.
a.CuO降低c(H+)浓度,不引入新杂质,过量的CuO可以过滤除去,故a正确;
b.CuCO3 降低c(H+)浓度,不引入新杂质,过量的CuCO3 可以过滤除去,故b正确;
c.CaCO3 引入钙离子,故c错误;
d.NaOH引入钠离子,故d错误.
故选:ab.
③由题目信息可知,氧气直接通入到铜粉与稀硫酸的混合物,发生反应生成硫酸铜与水,
反应方程式为2Cu+O2+2H2SO4
 2CuSO4+2H2O.
2CuSO4+2H2O.故答案为:2Cu+O2+2H2SO4
 2CuSO4+2H2O.
2CuSO4+2H2O.分析:(I)二氧化锰与浓盐酸反应生成氯化锰、氯气、水.实验一段时间后,C、D中有红棕色烟,红棕色烟应是FeCl3,即氯气与物质C反应生成FeCl3,据此物质C.
(II)(1)由题目信息,实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,判断图2分液漏斗中装的液体.
(2)硝酸过量制得的硫酸铜晶体中含有硝酸铜.
(3)装置3中在尾气吸收装置之前连接集气瓶,通入氧气有利于氮氧化合物的吸收,同时起安全瓶作用.
(4)①高温灼烧固体应在坩埚中进行.
②加入甲物质,目的是调节PH值,使Fe3+转化Fe(OH)3沉淀,且不能引入新杂质.
③由题目信息可知,氧气直接通入到铜粉与稀硫酸的混合物,发生反应生成硫酸铜与水.
点评:考查学生对实验原理的理解、实验方案的评价、实验装置的理解与评价、常用化学用语、物质推断、实验条件控制等,难度中等,实验方案设计,应根据实验目的思考实验原理,根据实验原理中反应物的状态和反应条件确定试剂和装置,通过比较和评价优选最佳实验方案.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目