题目内容
下列关于各实验装置与对应现象或结论的叙述均正确的是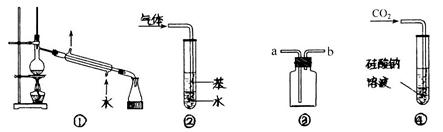
| A.装置①:可用于分离石油,分别得到汽油、煤油和柴油等各种纯净物 |
B.装置②:可用于吸收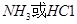 气体,并防止倒吸 气体,并防止倒吸 |
C.装置③:如果“a进b出”可用于收集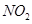 ,如果“b进a出”可用于收集 ,如果“b进a出”可用于收集 |
D.装置④:持续通入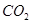 气体,现象是先出现白色沉淀,后变澄清 气体,现象是先出现白色沉淀,后变澄清 |
C
解析试题分析:A、汽油、煤油和柴油为不同烃组成的沸点在不同范围之间的混合物,不是纯净物,错误;B、苯的密度比水小,不能起到防倒吸的作用,应用四氯化碳,错误;C、NO2的密度比空气大,可用向上排空法收集,NH3的密度比空气小,可用向下排空法收集,正确;D、二氧化碳与硅酸钠反应生成硅酸白色沉淀,继续通入二氧化碳,沉淀不溶解,错误。
考点:本题考查物质的分离、实验安全的操作、气体的收集以及物质的性质的探讨。

练习册系列答案
相关题目
下列除杂质选用试剂和主要操作都正确的是
| | 物质 | 杂质 | 试剂 | 主要操作 |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | NaHCO3 | NH4Cl | — | 加热 |
| C | 铁粉 | 铜粉 | 稀硫酸 | 过滤 |
| D | 甲烷 | 乙烯 | 溴水 | 蒸馏 |
下列提纯物质的方法正确的是
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去CO中混有的CO2:用足量NaOH洗气 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
关于某溶液中所含离子的检验,下列判断正确的是
| A.加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO42- |
| B.向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中滴几滴新制的氯水,溶液变为红色,溶液中一定含有Fe2+ |
| C.用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+ |
| D.加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
为除去下列物质所含的杂质(括号内的物质),有关除杂试剂和操作合理的是
| A.乙醇(水):加氢氧化钙固体,过滤 |
| B.乙酸乙酯(乙酸):加氢氧化钠溶液,分液 |
| C.溴水(溴化钠):除杂过程中涉及的操作有:加CCl4,萃取、分液 |
| D.苯甲酸(苯甲酸钠):加稀硫酸,蒸馏 |
下列有关描述不正确的是
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.常温下,可以用铁或铝制容器盛装浓硫酸和浓硝酸 |
| D.检验某溶液中是否含有SO42-的方法是向该溶液中加入BaCl2溶液,再加入稀HNO3 |
从海水中提取镁的工艺流程如图所示。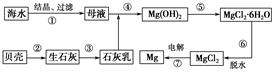
下列说法错误的是( )。
| A.用此法提取镁的优点之一是原料来源丰富 |
| B.步骤⑦电解MgCl2时阴极产生氯气 |
| C.步骤⑥可将晶体置于HCl气氛中脱水 |
| D.上述工艺流程中涉及化合、分解和复分解反应 |
下列叙述中不正确的是 ( )。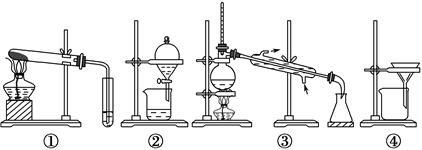
| A.可用装置①除去碳酸钠中的碳酸氢钠 |
| B.可用装置②分离汽油和水的混合物 |
| C.可用装置③从海水中蒸馏得到淡水 |
| D.可用装置④把胶体粒子从分散系中分离出来 |
