جâؤ؟ؤعبف
£¨12·ض£©جىب»ث®تابثہàزûسأث®µؤض÷زھہ´ش´،£´سجىب»ث®»ٌµأ؟ةزشزûسأµؤث®ز»°مذë¾¹³ء½µذü¸،خï،¢ة±¾ْدû¶¾µب²½ضè،£
£¨1£©³ء½µذü¸،خïزھشعث®ضذ¼سبëذُؤ¼ء£¬ب罫آءرخ¼سبëث®ضذؤـ´ïµ½¾»ث®ؤ؟µؤ£¬
شزٍتا £¨سأہë×س·½³جت½±يت¾£©،£
£¨2£©آبئّ؟ةسأسع×شہ´ث®ة±¾ْدû¶¾¼ء£¬½ل؛دہë×س·½³جت½؛حخؤ×ضہيسة ،£
£¨3£©ذآذحث®´¦ہي¼ء¸كجْثل¼ط (K2FeO4)¾كسذا؟µؤرُ»¯×÷سأ؛حذُؤ×÷سأ،£¹¤زµةد؟ةح¨¹زشدآء÷³جضئ±¸¸كجْثل¼ط£؛
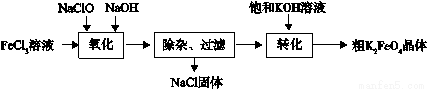
²éشؤ×تءد:¸كجْثلرخشعضذذش»ٍثلذشبـز؛ضذ»لضً½¥·ض½â£¬شع¼îذشبـز؛ضذخب¶¨،£
حê³ة،°رُ»¯،±¹³جضذµؤہë×س·½³جت½
،ُFe3+ + ،ُClO- +،ُ =،ُ FeO42- + ،ُCl- + ،ُ
،°×ھ»¯،±¹³جضذتµدضسةNa2FeO4ضئµأK2FeO4£¬تاہûسأ¶صك ذشµؤ²»ح¬،£
¢غ½ل؛د×تءدحê³ة´ضK2FeO4¾§جهµؤجل´؟£؛½«´ض²ْئ·سأ بـ½â£¬ب»؛َشظ¼سبë±¥؛حKOHبـز؛،¢ہنب´½ل¾§،¢¹آث،£
¢ـ¸كجْثل¼طµؤس¦سأ»¹شع²»¶دہ©ص¹ضذ،£بç؟ةضئ³ة¸كجْµç³ط£¬ µç³ط·´س¦خھ£؛
3Zn + 2K2FeO4 + 8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
·إµçت±£¬ص¼«·´س¦خھ£؛ ،£
£¨12·ض£©
£¨1£©Al3++3H2O Al(OH)3£¨½؛جه£©+ 3 H+ £¨2·ض£©
Al(OH)3£¨½؛جه£©+ 3 H+ £¨2·ض£©
£¨2£© Cl2 + H2O = HCl + HClO£¬ةْ³ةµؤHClOسذا؟رُ»¯ذش£¬¾كسذة±¾ْدû¶¾×÷سأ،£
£¨2·ض£©
£¨3£©¢ظ 2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl- +5H2O £¨2·ض£©
¢ع بـ½â £¨2·ض£©
¢غ د،KOHبـز؛£¬ £¨2·ض£©
¢ـ 2FeO42-+6e-+8H2O==2Fe(OH)3+10OH- £¨2·ض£©
،¾½âخِ،؟
تشجâ·ضخِ£؛£¨1£©آءرخ¼سبëث®ضذؤـ´ïµ½¾»ث®ؤ؟µؤ£¬تازٍخھآءہë×سث®½âµأاâرُ»¯آء½؛جه£¬¾كسذخü¸½×÷سأ£¬ہë×س·½³جت½تاAl3++3H2O Al(OH)3£¨½؛جه£©+ 3 H+
Al(OH)3£¨½؛جه£©+ 3 H+
£¨2£©آبئّبـسعث®ةْ³ة´خآبثل£¬Cl2 + H2O = HCl + HClO£¬´خآبثل¾كسذا؟رُ»¯ذش£¬سأہ´ة±¾ْدû¶¾£»
£¨3£©¢ظ¸ù¾فجâؤ؟µؤء÷³جح¼إذ¶د·´س¦خïضذسذاâرُ»¯ؤئ£¬ثùزش·´س¦خïµؤ؟ص°×´¦س¦تاOH-£¬شٍ²ْخïµؤ؟ص°×´¦س¦تاH2O£¬¸ù¾فµأت§µç×ستط؛م£¬إنئ½¸أ»¯ر§·½³جت½£¬´ً°¸تا2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl- +5H2O £»
¢ع،°×ھ»¯،±¹³جضذتµدضسةNa2FeO4ضئµأK2FeO4£¬تاہûسأ¶صكبـ½âذشµؤ²»ح¬£¬K2FeO4±بNa2FeO4µؤبـ½â¶بذ،£»
¢غ¸كجْثلرخشعضذذش»ٍثلذشبـز؛ضذ»لضً½¥·ض½â£¬شع¼îذشبـز؛ضذخب¶¨£¬ثùزش½«´ض²ْئ·سأد،KOHبـز؛بـ½â£»
¢ـ·إµçت±£¬½«»¯ر§ؤـ×ھ»¯خھµçؤـ£¬ص¼«·¢ةْ»¹ش·´س¦£¬µç¼«·½³جت½خھ2FeO42-+6e-+8H2O==2Fe(OH)3+10OH-
؟¼µم£؛؟¼²éہë×سµؤث®½â£¬آبئّµؤسأح¾£¬»¯ر§·½³جت½µؤإنئ½£¬µç»¯ر§شہيµؤس¦سأ

 أûجâ½ً¾يدµءذ´ً°¸
أûجâ½ً¾يدµءذ´ً°¸دآح¼ثùت¾µؤتµرé×°ضأ»ٍ²ظ×÷²»ؤـ´ïµ½تµرéؤ؟µؤµؤتا
|
| |
|
A£®إنضئ100 mL 0.1 mol /Lرخثل | B£® رéض¤AgCl؛حAg2Sµؤبـ½âذش | C£®²â¶¨ضذ؛ح·´س¦ µؤ·´س¦بب | D£®تµرéتزضئب، ²¢تص¼¯°±ئّ |