题目内容
【题目】KClO3和KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快。如图为反应速率v(ClO3-)随时间(t)的变化曲线。下列有关说法不正确的是( )

A. KClO3和KHSO3发生反应的氧化剂与还原剂的物质的量之比为1∶3
B. 反应开始阶段速率逐渐增大可能是c(H+)逐渐增高导致的
C. 反应后期速率逐渐减小的主要原因是c(ClO3-)、c(HSO3-))降低
D. 纵坐标为v(HSO3-)时的v-t曲线与原图曲线完全吻合
【答案】D
【解析】A. KClO3中Cl的化合价降低6,KClO3作氧化剂,KHSO3中S的化合价升高2,KHSO3作还原剂,根据得失电子数目相等可得KClO3和KHSO3发生反应的氧化剂与还原剂的物质的量之比为1∶3,故A正确;B. 反应开始阶段速率逐渐增大可能是c(H+)逐渐增高导致的,故B正确;C. 反应后期速率逐渐减小的主要原因是c(ClO3-)、c(HSO3-))降低,故C正确;D. KClO3和KHSO3的物质的量之比为1∶3,对应KClO3和KHSO3的反应速率之比为1∶3,所以纵坐标为v(HSO3-)时的v-t曲线与原图曲线不会完全吻合,故D不正确。故选D。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案【题目】元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥIA | VIIA | 0 |
2 | 3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne |
3 | 11 Na | 12Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar |
(1)请从上表中查出关于硼元素的一条信息: .
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的相同.
(3)第11号元素与第17号元素组成的化合物是 , 构成该物质的微粒是(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题: 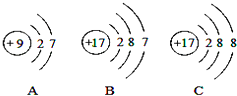
①A、B、C中属于同种元素的粒子是;
②A和B两种粒子的相同,所以它们具有相似的化学性质.