题目内容
0.2mol有机物与1.6molO2在密闭容器中恰好完全反应后的产物为CO2和H2O(g),产物先通过足量的浓H2SO4质量增加21.6g,再通过碱石灰被完全吸收,质量增加44g。
小题1:试推断该有机物的分子式(要求写出过程)
小题2:写出该有机物可能有的同分异构体的结构简式,并用系统命名法命名
小题1:试推断该有机物的分子式(要求写出过程)
小题2:写出该有机物可能有的同分异构体的结构简式,并用系统命名法命名
小题1:①浓硫酸增重21.6g,则生成物水的质量是21.6g,物质的量为
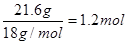 ,其中含有的氧原子是1.2mol。
,其中含有的氧原子是1.2mol。②碱石灰增重44g,则生成物CO2的质量就是44g,物质的量为1mol,其中含有的氧原子是2mol。
③参加反应的氧气是1.6mol,所以根据原子守恒可判断有机物中不含氧原子。
④根据碳原子和氢原子守恒可知,该有机物的分子式为C5H12。
小题2:有机物是戊烷,有三种同分异构体,分别是①正戊烷,结构简式为CH3CH2CH2CH2CH3;
②2-甲基丁烷结构简式为CH3CH(CH3)CH2CH3;③2,2-二甲基丙烷,结构简式为C(CH3) 4。
考查有机物分子式和结构式的判断和同分异构体的书写以及命名等。
根据有机物燃烧的产物并结合原子守恒可计算出碳原子和氢原子的个数,然后再根据质量守恒定律可判断是否含有氧原子以及含有几个氧原子;烷烃同分异构体的书写一般遵循主链由长到短,支链由整到散,位置由心到边,排列邻、对、间的原则。而烷烃的命名关键是找准含碳原子数最多的碳链作为主链,而编号则要离支链最近的一端开始。
根据有机物燃烧的产物并结合原子守恒可计算出碳原子和氢原子的个数,然后再根据质量守恒定律可判断是否含有氧原子以及含有几个氧原子;烷烃同分异构体的书写一般遵循主链由长到短,支链由整到散,位置由心到边,排列邻、对、间的原则。而烷烃的命名关键是找准含碳原子数最多的碳链作为主链,而编号则要离支链最近的一端开始。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
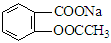 转变为
转变为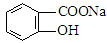 方法为 ( )
方法为 ( )