题目内容
【题目】向40mL某AlCl3溶液中滴加2molL﹣1的NaOH溶液时,得到Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题: 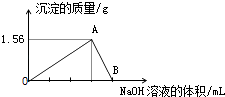
(1)图中A点表示的沉淀是 , 其物质的量是 .
(2)反应至A点时消耗NaOH溶液体积为 .
(3)图中B点溶液中溶质有 .
(4)AlCl3溶液的浓度为
(5)O点到B点反应的总离子方程式可表示为 .
【答案】
(1)Al(OH)3;0.02mol
(2)30mL
(3)NaCl、NaAlO2
(4)0.5mol/L
(5)Al3++4OH﹣=AlO2﹣+2H2O
【解析】解:(1)开始AlCl3与NaOH发生反应Al3++3OH﹣=Al(OH)3↓生成Al(OH)3沉淀,NaOH量逐渐增多,Al(OH)3量逐渐增大,到A点时氢氧化钠将AlCl3恰好完全沉淀时,Al(OH)3沉淀达到最大量,其物质的量为 ![]() =0.02mol,所以答案是:Al(OH)3;0.02mol;(2)根据Al3++3OH﹣=Al(OH)3↓可知,消耗NaOH物质的量=0.02mol×3=0.06mol,消耗NaOH溶液体积为
=0.02mol,所以答案是:Al(OH)3;0.02mol;(2)根据Al3++3OH﹣=Al(OH)3↓可知,消耗NaOH物质的量=0.02mol×3=0.06mol,消耗NaOH溶液体积为 ![]() =0.03L,即为30mL,所以答案是:30mL;(3)Al(OH)3沉淀达到最大量后,再加NaOH溶液发生反应:Al(OH)3+OH﹣=AlO2﹣+2H2O,沉淀量开始逐渐减少,到B点时Al(OH)3与NaOH恰好完全反应生成NaAlO2 , 沉淀完全溶解消失,B点溶液中溶质有NaCl、NaAlO2 , 所以答案是:NaCl、NaAlO2;(4)根据Al原子守恒n[AlCl3]=n[Al(OH)3]=0.02mol,AlCl3溶液的浓度为
=0.03L,即为30mL,所以答案是:30mL;(3)Al(OH)3沉淀达到最大量后,再加NaOH溶液发生反应:Al(OH)3+OH﹣=AlO2﹣+2H2O,沉淀量开始逐渐减少,到B点时Al(OH)3与NaOH恰好完全反应生成NaAlO2 , 沉淀完全溶解消失,B点溶液中溶质有NaCl、NaAlO2 , 所以答案是:NaCl、NaAlO2;(4)根据Al原子守恒n[AlCl3]=n[Al(OH)3]=0.02mol,AlCl3溶液的浓度为 ![]() =0.5mol/L,所以答案是:0.5mol/L;(5)由反应Al3++3OH﹣=Al(OH)3↓、Al(OH)3+OH﹣=AlO2﹣+2H2O可知,铝离子与氢氧根离子的总反应为:Al3++4OH﹣=AlO2﹣+2H2O,
=0.5mol/L,所以答案是:0.5mol/L;(5)由反应Al3++3OH﹣=Al(OH)3↓、Al(OH)3+OH﹣=AlO2﹣+2H2O可知,铝离子与氢氧根离子的总反应为:Al3++4OH﹣=AlO2﹣+2H2O,
所以答案是:Al3++4OH﹣=AlO2﹣+2H2O.

 阅读快车系列答案
阅读快车系列答案