题目内容
向27.2Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法正确的是
| A.Cu与Cu2O 的物质的量之比为1:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
D
39.2g沉淀是氢氧化铜,物质的量是0.4mol。如果设铜和氧化亚铜的物质的量分别是x和y,则64x+144y=27.2g和x+2y=0.4mol,解得x=0.2mol,y=0.1mol,所以选项A不正确;反应中共转移电子是0.2mol×2+0.1mol×2=0.6mol,所以根据电子的得失守恒可知,生成NO是0.6mol÷3=0.2mol,但体积不一定是4.48L,选项C不正确;生成物硝酸钠是1mol,所以原硝酸的物质的量是1mol+0.2mol=1.2mol,浓度是1.2mol÷0.5L=2.4mol/L,选项B不正确;生成硝酸铜是0.4mol,所以剩余硝酸是1.2mol-0.4mol×2-0.2mol=0.2mol,选项D正确,答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 的浓度为
的浓度为  mol
mol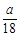 mol
mol mol
mol mol
mol