��Ŀ����
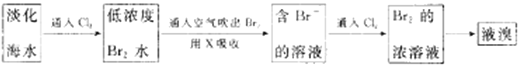
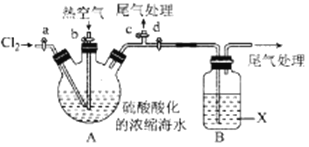
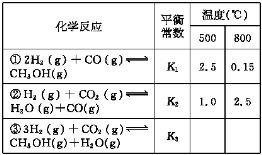
����Ŀ���״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�Ʊ��״����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ�����±���ʾ��
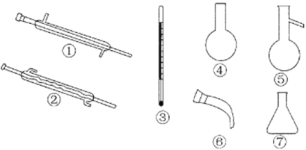
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
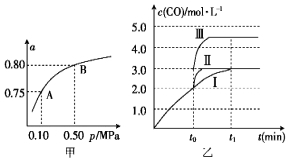
��2��ij�¶��·�Ӧ����H2��ƽ��ת������a������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ����ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K��A�� K��B�����>����<����=������
��3���ݷ�Ӧ���������Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����500 ��ʱ��÷�Ӧ����ijʱ��ʱ��H2��g����CO2��g����CH3OH��g����H2O��g����Ũ����mol��L��1���ֱ�Ϊ0.8��0.1��0.3��0.15�����ʱv�� v�� ��� > ����=����<������
��4����3 L�ݻ��ɱ���ܱ������з�����Ӧ������֪c��CO�� ��t����Ӧʱ�����仯��������ͼ����ʾ������t0ʱ�̷ֱ�ı�һ����������������Ϊ��������������������������Ϊ������ʱ���ı�������� ������������Ϊ������ʱ���ı������ ��
���𰸡���ÿ����������1��������2��=��3��K1K2����
��4������������������������������ѹ����2L
��������
�����������1������ͼ�����ݣ���Ӧ��ƽ�ⳣ�����¶���������ƽ��������У�����Ӧ�����ȷ�Ӧ��
��2������ƽ�ⳣ�����¶ȱ仯������ѹǿ�仯������ͼ����ƽ��״̬��A�䵽Bʱ��ѹǿ�ı䣬�¶Ȳ��䣬����ƽ�ⳣ�����䣻
��3�����ݷ�Ӧ��+�ڵõ���Ӧ�ۣ�����ƽ�ⳣ��K3=K1��K2����500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��g����CO2��g����CH3OH��g����H2O��g����Ũ����mol��L��1��0.8��0.1��0.3��0.15����Ũ����Q��![]() ��K=2.5����Ӧ������У�V����V�棻
��K=2.5����Ӧ������У�V����V�棻
��4��ͼ��������ߢ�仯Ϊ���ߢ������̷�Ӧ�ﵽƽ���ʱ�䣬���ﵽ��ͬƽ��״̬������ǿɱ���Ǻ�ѹ������˵���ı���Ǽ����˴����������ߢ��Ϊ���ߢ�ʱһ����̼���ʵ�������Ӧ�������������ķ�Ӧ���ɱ����������������Ũ�ȳɷ��ȣ��������ʵ������䣬���ߢ����Ϊ3L��һ����̼Ũ��Ϊ3mol/L���ı���������Ϊ���ߢ�һ����̼Ũ��Ϊ4.5mol/L�������ѹ�����Ϊ��3��V=4.5��3��V=2L�����Խ��������������ѹ����2L������

 ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д� A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д�