题目内容
下列属于正确的水解离子方程式的是( )
|
| A. | NH4++H2O⇌NH3•H2O+H+ | B. | H2O+H2O⇌H3O++OH﹣ |
|
| C. | CO32﹣+2H2O⇌H2CO3+2OH﹣ | D. | Fe3++3H2O⇌Fe(OH)3↓+3H+ |
考点:
盐类水解的原理;离子方程式的书写.
专题:
盐类的水解专题.
分析:
根据盐类方程式的书写规则判断.
盐类水解方程式的书写规则为:
1、盐类水解一般很微弱,要写“⇌”,产物不标“↓”或“↑”.
2、多元弱酸盐的水解是分步进行的且一步比一步难,因此,水解方程式要分步写.
3、多数弱碱阳离子也是分步水解的,但一般以总反应式表示.
解答:
解:A、该方程式符合书写规则,故A正确.
B、该方程式是电离方程式,故B错误.
C、多元弱酸盐的水解是分步进行,故C错误.
D、盐类水解一般很微弱,产物不标“↓”,故D错误.
故选A
点评:
盐类水解方程式的书写规则为:
1、盐类水解一般很微弱,要写“⇌”,产物不标“↓”或“↑”.
2、多元弱酸盐的水解是分步进行的且一步比一步难,因此,水解方程式要分步写.
3、多数弱碱阳离子也是分步水解的,但一般以总反应式表示.

已知4NH3(g)+5O2(g)═4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系式为( )
|
| A. | 4v(NH3)=5v(O2) | B. | 5v(O2)=6v(H2O) | C. | 2v(NH3)=3v(H2O) | D. | 4v(O2)=5v(NO) |
在密闭容器中,aA(气)⇌bB(气)达平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,下列说法正确的是( )
|
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率减少了 |
|
| C. | 物质B的质量分数增加了 | D. | a>b |
体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,是该碱溶液的pH等于( )
|
| A. | 9.0 | B. | 9.5 | C. | 10.5 | D. | 11.0 |
下列有关热化学方程式的叙述中,正确的是( )
|
| A. | 含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(1)△H=+57.3kJ/mol |
|
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
|
| C. | 已知2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ |
|
| D. | 已知C(s)+O2(g)=CO2(g)△H1;C(s)+ |
 2SO3(g),△H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是 ( )
2SO3(g),△H<0。现有三个体积相同的密闭容器I、II、III,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是 ( )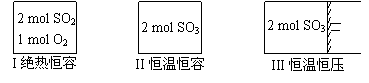

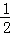 O2(g)=CO(g)△H2,则△H1<△H2
O2(g)=CO(g)△H2,则△H1<△H2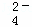 、Cl﹣、H+的物质的量浓度分别是多少?
、Cl﹣、H+的物质的量浓度分别是多少?