题目内容
25℃时,在含有Pb2+ 、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+ (aq) 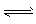 Sn2+ (aq)+Pb(s) △H<0,体系中c(Pb2+ )和c(Sn2+)的变化关系如图所示。下列判断正确的是
Sn2+ (aq)+Pb(s) △H<0,体系中c(Pb2+ )和c(Sn2+)的变化关系如图所示。下列判断正确的是
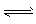 Sn2+ (aq)+Pb(s) △H<0,体系中c(Pb2+ )和c(Sn2+)的变化关系如图所示。下列判断正确的是
Sn2+ (aq)+Pb(s) △H<0,体系中c(Pb2+ )和c(Sn2+)的变化关系如图所示。下列判断正确的是 
[ ]
A.往平衡体系中加入等体积的水,平衡向右移动
B.若该反应在30℃时进行,则平衡时c(Sn2+ )增大
C.若该反应在20℃时进行,则达到平衡所需要的时间t<t0
D.25℃时.该反应的平衡常数K=2.2
B.若该反应在30℃时进行,则平衡时c(Sn2+ )增大
C.若该反应在20℃时进行,则达到平衡所需要的时间t<t0
D.25℃时.该反应的平衡常数K=2.2
D

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )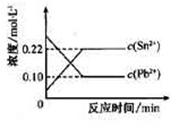
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
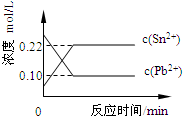 (2011?福建)25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
(2011?福建)25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )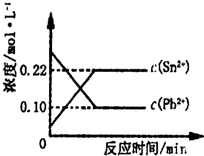 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s)△H>0,体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s)△H>0,体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )