题目内容
【题目】NH3和纯净的O2在一定条件下发生反应:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g),现向一容积不变的2L密闭容器中充入4molNH3和3molO2,4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
2N2(g)+6H2O(g),现向一容积不变的2L密闭容器中充入4molNH3和3molO2,4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
A. V(NH3)=0.250moL·L-1·min-1 B. V(H2O)=0.375moL·L-1·min-1
C. V(N2)=0.125moL·L-1·min-1 D. V(O2)=0.225moL·L-1·min-1
【答案】D
【解析】设反应消耗的NH3为4xmol/L,根据方程式可知
4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g)
2N2(g)+6H2O(g)
起始浓度(mol/L) 2 1.5 0 0
反应浓度(mol/L) 4x 3x 2x 6x
平衡浓度(mol/L) 2-4x 1.5-3x 2x 6x
4min后,测得生成的水蒸气占混合气体体积的40%,则6x/(3.5+x)×100%=40%,解得:x=0.25,则
A、用氨气表示的反应速率为:v(NH3)=1mol/L÷4min=0.250molL-1min-1,A正确;B、反应速率之比是相应的化学计量数之比,则V(H2O)=0.375moL·L-1·min-1,B正确;C、V(N2)=0.125moL·L-1·min-1,C正确;D、V(O2)= 0.250molL-1min-1×3/4=0.1875molL-1min-1,D错误;答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在一定条件下,N2O分解的部分实验数据如下( )
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/molL-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
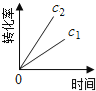
下图能正确表示该反应有关物理量变化规律的是( )
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
A. B.
B. C.
C. D.
D.