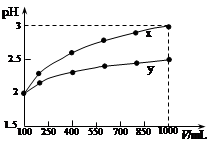题目内容
(3分)25℃时,有下列四组溶液①0.1mol/L醋酸溶液,②0.1mol/L的盐酸,③pH=13的氢氧化钠溶液,④pH=13的氨水
(1)溶液中的c(H+)大小关系是 (填序号,下同)。
(2)其中水的电离程度最大的是 。
(3)取等体积的③和④的溶液分别稀释100倍,稀释后溶液的pH关系为③ ④(填“>”、“=”、“<”)。
(1)溶液中的c(H+)大小关系是 (填序号,下同)。
(2)其中水的电离程度最大的是 。
(3)取等体积的③和④的溶液分别稀释100倍,稀释后溶液的pH关系为③ ④(填“>”、“=”、“<”)。
(3分)(1)②>①>③=④ (2)① (3)<
(1)醋酸是弱酸,盐酸是强酸,氢氧化钠是强碱,氨水是弱碱,溶液中的c(H+)大小关系是②>①>③=④。
(2)酸或碱中氢离子或OH-浓度越大,对水的电离抑制程度越大。①氢离子浓度最小,所以水的电离程度最大的是①。
(3)氨水是弱碱,存在电离平衡,稀释促进电离,所以稀释后氨水的碱性强于氢氧化钠的,即氨水的pH大于氢氧化钠的pH。
(2)酸或碱中氢离子或OH-浓度越大,对水的电离抑制程度越大。①氢离子浓度最小,所以水的电离程度最大的是①。
(3)氨水是弱碱,存在电离平衡,稀释促进电离,所以稀释后氨水的碱性强于氢氧化钠的,即氨水的pH大于氢氧化钠的pH。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目