题目内容
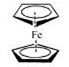
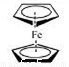
二茂铁(结构如图)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到。反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O
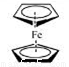
二茂铁的熔点为172~173℃,在100℃开始升华。能溶于乙醚、二甲亚砜等非极性溶剂,不溶于水,对碱和非氧化性酸稳定。制备的步骤如下:
步骤1.在150mL的三颈瓶中加入25g细粉末状KOH和60mL无水乙醚,通入氮气并搅拌约10分钟使之尽可能溶解,然后加入5.5 mL环戊二烯,再搅拌10分钟。
步骤2. 向烧杯中加入25 mL二甲亚砜和6.5g新制的无水氯化亚铁,微热至40℃并搅拌使其溶解,然后加入滴液漏斗中。
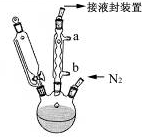
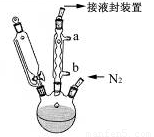
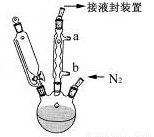
步骤3. 按图所示的装置装配好仪器,打开滴液漏斗的活塞,缓慢将氯化亚铁等加入三颈瓶中,并继续搅拌1小时。
步骤4. 反应结束后,将混合物倒入100mL 18%的盐酸溶液,将烧杯放在冰浴中冷却,搅拌约10分钟,使结晶完全。
步骤5. 抽滤,将获得的产品以冷水洗涤2~3次,低温风干得到粗制的二茂铁。
(1)步骤1中通入N2的目的可能是 。
(2)步骤2中,滴液漏斗侧边的玻璃导管的作用是 。
(3)实验装置中,冷凝管通水,水应从 口进(选填a或b)。
(4)步骤4将反应后的混合物倒入盐酸中,发生主要反应的离子方程式是 。
(5)步骤5用冷水洗涤是因为 ,因此可采用 的方法,进一步提纯二茂铁。
(每空2分,共12分)
(1)排出三颈瓶内的空气
(2)均衡漏斗内压强,便于液体放出(3)b
(4)H+ + OH- = H2O
(5)二茂铁易于升华 加热升华
【解析】用氮气赶空气,滴液漏斗侧边的玻璃导管的作用是排出三颈瓶内的空气。冷凝管应该下进上出。将反应后的混合物倒入盐酸中发生中和反应,用冷水洗涤是因为二茂铁易于升华,用加热升华的方法提纯二茂铁。

 名校课堂系列答案
名校课堂系列答案