题目内容
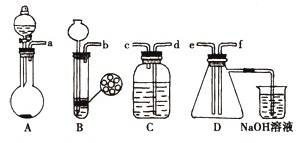 已知实验室制取H2S的实验原理为FeS(块状)+H2SO4═FeSO4+H2S↑.
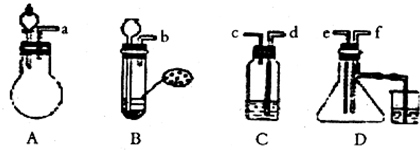
已知实验室制取H2S的实验原理为FeS(块状)+H2SO4═FeSO4+H2S↑.根据图中A~D的实验装置和试剂进行实验:
(1)装置A是由双孔塞、玻璃导管、
(2)组装一套制取二氧化硫气体的装置,并证明二氧化硫既有氧化性又有还原性.制备SO2的实验原理:
Na2SO3(粉末)+H2SO4(70%)═Na2SO4+SO2↑+H2O.
①按实验装置连接顺序:把a→f各导管口连接起来,正确的顺序是
②C装置中的溶液是
(3)D中产生的现象是
(4)烧杯中发生反应的离子方程式为
分析:(1)根据装置A中各仪器的构造进行解答;
(2)①先判断硫化氢、二氧化硫的发生装置分别为注重B、装置A,然后按照检验二氧化硫的还原性(装置C)、氧化性(装置D),最后为尾气吸收装置,据此进行连接装置;
②根据装置C作用是检验二氧化硫的还原性来选择使用的试剂;
(3)装置D中硫化氢与二氧化硫发生反应生成淡黄色的单质硫;
(4)二氧化硫和硫化氢都有毒,容易造成大气污染,需要进行尾气吸收,D中为气体与NaOH的反应.
(2)①先判断硫化氢、二氧化硫的发生装置分别为注重B、装置A,然后按照检验二氧化硫的还原性(装置C)、氧化性(装置D),最后为尾气吸收装置,据此进行连接装置;
②根据装置C作用是检验二氧化硫的还原性来选择使用的试剂;
(3)装置D中硫化氢与二氧化硫发生反应生成淡黄色的单质硫;
(4)二氧化硫和硫化氢都有毒,容易造成大气污染,需要进行尾气吸收,D中为气体与NaOH的反应.
解答:解:(1)装置A是由双孔塞、玻璃导管及分液漏斗、圆底烧瓶组装起来的,故答案为:分液漏斗;圆底烧瓶;
(2)①FeS不溶解于水,而Na2SO3可溶于水,所以制取H2S的装置用B,而制SO2的装置为A;为了证明SO2的氧化性,应该在D装置的锥形瓶中混合两气体;为了证明其还原性,可以C试剂瓶中注放氧化剂,例如酸性KMnO4溶液或溴水等;很明显D装置中的碱溶液起到尾气吸收的作用,所以装置连接顺序为adcefb,
故答案为:dcef(或adcfeb);
②装置C中可以加入具有氧化性且能够有明显现象的试剂,如酸性高锰酸钾溶液、溴水等,作用为检验二氧化硫的还原性,发生氧化还原反应,生成硫酸根离子,体现其还原性,故答案为:酸性高锰酸钾溶液(或溴水);还原;
③装置D的作用是证明二氧化硫具有氧化性,二氧化硫能够与硫化氢发生氧化还原反应生成单质硫,装置D内壁有淡黄色固体生成,
故答案为:内壁出现淡黄色固体;氧化;
(4)硫化氢和二氧化硫都有毒,会污染大气,不能直接排放,需要使用尾气吸收装置,所以D旁的烧杯盛放的NaOH溶液的作用为吸收过量的SO2或H2S,防止污染空气,发生的离子反应为2OH-+SO2=SO32-+H2O、H2S+2OH-=S2-+2H2O,故答案为:2OH-+SO2=SO32-+H2O、H2S+2OH-=S2-+2H2O.
(2)①FeS不溶解于水,而Na2SO3可溶于水,所以制取H2S的装置用B,而制SO2的装置为A;为了证明SO2的氧化性,应该在D装置的锥形瓶中混合两气体;为了证明其还原性,可以C试剂瓶中注放氧化剂,例如酸性KMnO4溶液或溴水等;很明显D装置中的碱溶液起到尾气吸收的作用,所以装置连接顺序为adcefb,
故答案为:dcef(或adcfeb);
②装置C中可以加入具有氧化性且能够有明显现象的试剂,如酸性高锰酸钾溶液、溴水等,作用为检验二氧化硫的还原性,发生氧化还原反应,生成硫酸根离子,体现其还原性,故答案为:酸性高锰酸钾溶液(或溴水);还原;
③装置D的作用是证明二氧化硫具有氧化性,二氧化硫能够与硫化氢发生氧化还原反应生成单质硫,装置D内壁有淡黄色固体生成,
故答案为:内壁出现淡黄色固体;氧化;
(4)硫化氢和二氧化硫都有毒,会污染大气,不能直接排放,需要使用尾气吸收装置,所以D旁的烧杯盛放的NaOH溶液的作用为吸收过量的SO2或H2S,防止污染空气,发生的离子反应为2OH-+SO2=SO32-+H2O、H2S+2OH-=S2-+2H2O,故答案为:2OH-+SO2=SO32-+H2O、H2S+2OH-=S2-+2H2O.
点评:本题考查含硫的化合物的相关性质及实验,题目难度中等,解题关键是明确实验目的、实验原理,有利于培养学生的分析、理解能力及灵活应用所学知识解决实际问题的能力.

练习册系列答案
相关题目