题目内容
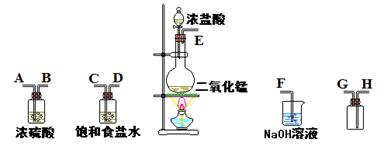
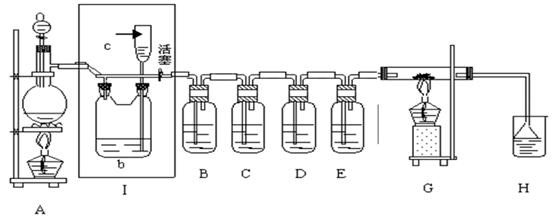
(12分)(1)氯气可溶于水,常温下,1体积水中溶解2体积的氯气,溶于水的氯气一部分与水反应,该化学方程式是 。
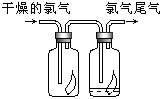
(2)多余氯气常用NaOH溶液吸收,写出化学方程式
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是____________;过一会儿,溶液颜色逐渐褪去,起作用的成分是____________;往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是________________。
(2)多余氯气常用NaOH溶液吸收,写出化学方程式
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是____________;过一会儿,溶液颜色逐渐褪去,起作用的成分是____________;往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是________________。
(1)(3分)Cl2 + H2O =" HCl" +HClO
(2)(3分)Cl2 + 2NaOH =" NaCl" +NaClO + H2O
(3)(6分)每空2分HCl(H+); HClO; HCl(Cl-)
(2)(3分)Cl2 + 2NaOH =" NaCl" +NaClO + H2O
(3)(6分)每空2分HCl(H+); HClO; HCl(Cl-)
试题分析:(1)氯气与水反应的化学方程式为Cl2+H2O=HCl+HClO;
(2)氯气与NaOH溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O
(3)氯气是氯气溶于水后形成的溶液,而溶于水的氯气只占一部分,因此氯水中的主要成分有H+、Cl-、ClO-、HClO、Cl2、H2O。使紫色石蕊试纸变红的应为酸,故起作用的成分应为H+;褪色主要是HClO的强氧化性;产生的白色沉淀为AgCl,因此起作用的为Cl-。
点评:本题考查了氯气的性质,属于基础题。只要掌握好课本中涉及到的氯气的基本性质,即可很好的解答此题。另外,需注意液氯与氯水的区别。

练习册系列答案
相关题目