题目内容
7.下列6种试剂:①烧碱溶液 ②金属钠 ③浓硝酸 ④葡萄糖溶液 ⑤氯化铝溶液 ⑥氨水,可以直接盛放在带磨口玻璃塞的无色试剂瓶中的是( )| A. | ①和③ | B. | ②和④ | C. | ③和⑥ | D. | ④和⑤ |
分析 玻璃中含有二氧化硅,能和强碱反应生成粘性的可溶性硅酸盐,所以带有磨口塞的玻璃棒不能盛放碱性溶液,据此分析解答.
解答 解:①烧碱溶液能与玻璃中的二氧化硅反应生成具有粘和合性的硅酸钠,容易将瓶口和瓶塞粘结在一起,故烧碱溶液盛放在带橡皮塞的玻璃瓶中,故①错误;
②因金属钠能与空气中的氧气和水反应,须贮存在煤油中隔离空气,故②错误;
③因浓硝酸易分解,须存放在棕色试剂瓶中,故③错误;
④葡萄糖溶液与二氧化硅不反应,可直接盛放在带磨口玻璃塞的无色试剂瓶中,故④正确;
⑤氯化铝溶液水解显酸性,与二氧化硅不反应,直接盛放在带磨口玻璃塞的无色试剂瓶中,故⑤正确;
⑥氨水呈碱性,不能用带磨口玻璃塞的无色试剂瓶保存,故⑥错误;
故选D.
点评 本题考查了化学试剂的存放,明确物质的性质是解本题关键,根据盐溶液的酸碱性来分析解答,题目难度不大.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
19.下列反应的离子方程式中正确的是( )
| A. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++H2O | |
| B. | 小苏打溶液中加入少量的石灰水:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O | |
| C. | 往Ca(ClO)2溶液中通入少量的SO2:Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓ | |
| D. | 碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH=Ca2++2CH3COO-+2CO2↑+2H2O |
20.熔点最低的金属洒落地上,用来处理的物质是( )
| A. | O2 | B. | S | C. | Cl2 | D. | I2 |
2.二元酸H2A在水中的电离情况是:H2A=H++HA-和HA-?H++A2-,则下列物质的水溶液中粒子浓度之间存在的关系错误的是( )
| A. | NaHA:c(Na+)>c(HA-)>c(H+)>c(OH-) | B. | NaHA:c(Na+)=c(A2-)+c(HA-)+c(H2A) | ||
| C. | Na2A:c(Na+)>c(A2-)>c(OH-)>c(H+) | D. | H2A:c(H+)=c(HA-)+2 c(A2-)+c(OH-) |
12.下列各组物质的性质比较,不正确的是( )
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>HBr>HI | ||
| C. | 酸性强弱:H4SiO4<H2CO3<H2SO4 | D. | 熔点:I2>Br2>Cl2 |
19.反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加H2的浓度 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入N2(N2不参加反应)使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积增大 |
16.关于水的离子积常数,下列说法不正确的是( )
| A. | 100℃水中,c(H+)•c(OH-)=1×10-14 | |
| B. | 纯水中,25℃时,c(H+)•c(OH-)=1×10-14 | |
| C. | 25℃时,任何以水为溶剂的稀溶液中c(H+)•c(OH-)=1×10-14 | |
| D. | KW值随温度升高而增大 |
17.下列离子方程式书写正确的是( )
| A. | 用Pt电极电解少量的MgC12溶液:2H2O+2Cl- $\frac{\underline{\;通电\;}}{\;}$H2↑+C12↑+2OH- | |
| B. | H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑ | |
| C. | 硫酸氢钠溶液中加入少量氢氧化钡溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| D. | FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O |
 双草酸酯(CPPO)是冷光源发光制料的主要成分,结构简式如图所示.请回答下列问题:
双草酸酯(CPPO)是冷光源发光制料的主要成分,结构简式如图所示.请回答下列问题: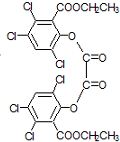 +4NaOH→2
+4NaOH→2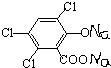 +NaOOCCOONa+2CH3CH2OH;
+NaOOCCOONa+2CH3CH2OH;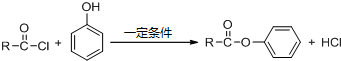 ,CPPO可由芳香族化合物A和脂肪族化合物B在一定条件下合成,A的结构简式
,CPPO可由芳香族化合物A和脂肪族化合物B在一定条件下合成,A的结构简式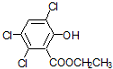 ,写出合成CPPO的化学方程式ClOC-COCl+2
,写出合成CPPO的化学方程式ClOC-COCl+2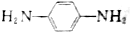 与脂肪族化合物B可聚合成性能良好,有使用价值的树脂,写出该聚合反应的方程式n
与脂肪族化合物B可聚合成性能良好,有使用价值的树脂,写出该聚合反应的方程式n +2nHCl.
+2nHCl.