题目内容
V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
| | Y | V | | |
| X | | | | W |
Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素。V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成。下列说法正确的是( )。
A.原子半径:X>Y>V>W
B.X、W的质子数之和与最外层电子数之和的比值为2∶1
C.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键
D.少量Z的单质与过量W的单质可化合生成ZW2
C
解析

练习册系列答案
相关题目
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素。下列说法正确的是
| | | | | | | X |
| Y | | Z | | | | W |
A.工业上电解ZW3饱和溶液冶炼金属Z
B.元素X的最高正价与W的最高正价相同
C.简单离子半径的大小顺序:r(Y+)>r(X—)
D.Y、W的最高价氧化物的水化物均能溶解金属Z
简单原子的原子结构可用下图形象地表示: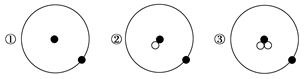
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是
a.①②③互为同位素
b.①②③由同种元素构成
c.①②③是三种化学性质不同的粒子
d.①②③具有相同的质量数
e.①②③具有相同的质量
f.①②③是三种不同的原子
| A.a、b、f | B.b、c、d | C.a、d、e | D.a、e、f |
X、Y、Z、W为短周期主族元素,原子序数依次增大,X的族序数是周期数的2倍,Y的气态氢化物与最高价氧化物水化物可形成盐,Z的最外层电子数与其电子总数比为3∶8,下列说法正确的是( )
| A.X、Y、W的最高价含氧酸酸性顺序:Y>W>X |
| B.Z、W可形成ZW2的化合物,属于离子化合物 |
| C.离子半径:Z>W>Y |
| D.气态氢化物的稳定性:Z>W |
下图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
| A.N、Z两种元素的离子半径相比前者较大 |
| B.M、N两种元素的气态氢化物的稳定性相比后者较强 |
| C.X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应 |
| D.工业上常用电解Y和N形成的化合物的熔融态制取Y的单质 |
He可以作为核聚变材料,科学家已经探明月球上有大量的3He存在,以下关于3He的说法正确的是( )
①比4He少一个电子
②比4He少一个质子
③与4He互为同素异形体
④3He的质量数为3,所以He元素的相对原子质量为3
⑤体积相同、密度相同的3He与HD具有相同的中子数
⑥是4He的同位素
| A.①③ | B.③⑤ | C.④⑥ | D.⑤⑥ |
某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是 ( )。
| A.电子排布式为1s22s22p63s23p63d34s2 |
| B.该元素为V |
| C.该元素为ⅡA族元素 |
| D.该元素位于d区 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B.由水溶液的酸性:HCl>H2S,可推断元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以作半导体材料 |
| D.Cs和Ba分别位于第六周期ⅠA和ⅡA族,则碱性:CsOH>Ba(OH)2 |
下列说法中正确的是( )。
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为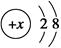 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为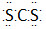 |
| D.中子数为18的氯原子可表示为18Cl |