题目内容
配制100mL1.0mol?L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( )A.容量瓶使用前有少量蒸馏水
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.在转移过程中有溶液撒在外面
D.定容时俯视确定凹液面与刻度线相切
【答案】分析:分析具体操作对溶质的物质的量或对溶液的体积的影响,根据c=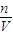 进行具体判断.
进行具体判断.
解答:解:A、配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故A不符合;
B、未用蒸馏水洗涤烧杯和玻璃棒,少量氢氧化钠粘在烧杯壁和玻璃棒上,移入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故B不符合;
C、转移过程中有溶液撒在外面,入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故C不符合;
D、定容时俯视凹液面,导致所配溶液的体积偏小,所配溶液浓度偏高,故D符合.
故选:D.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,误差分析关键关键清楚溶液配制原理.分析不当操作对n或V的影响,通过c= 进行计算判断.
进行计算判断.
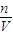 进行具体判断.
进行具体判断.解答:解:A、配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故A不符合;
B、未用蒸馏水洗涤烧杯和玻璃棒,少量氢氧化钠粘在烧杯壁和玻璃棒上,移入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故B不符合;
C、转移过程中有溶液撒在外面,入容量瓶内氢氧化钠的物质的量减小,所配溶液浓度偏低,故C不符合;
D、定容时俯视凹液面,导致所配溶液的体积偏小,所配溶液浓度偏高,故D符合.
故选:D.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,误差分析关键关键清楚溶液配制原理.分析不当操作对n或V的影响,通过c=
 进行计算判断.
进行计算判断. 
练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目

